Considere a estrutura electrónica do átomo de ferro, bem como a sua posição na tabela periódica. Identificar as propriedades físicas e químicas chave do elemento, o campo de utilização.
A situação na SS
O ferro é um d-8 grupo (grupo de transição) elemento. 26 tem um número de série, de massa atómica relativa – 56, no seu átomo contém 26 protões, electrões, 26 e 30 neutrões. Esse metal tem uma elevada reactividade, exibe propriedades redutoras. estado de oxidação típica 2, 3.
Características da estrutura do átomo
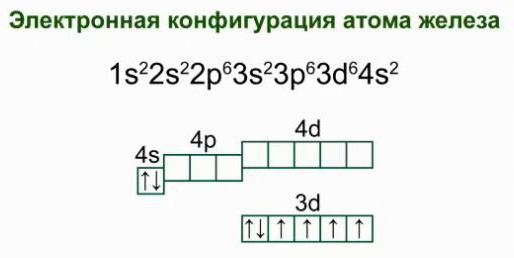
O que é uma electrónica diagrama da estrutura de um átomo de ferro? Se considerarmos a distribuição dos elétrons nos níveis de energia, obtemos a seguinte encarnação:
2e; 8e; 14 e; 2e. Uma tal estrutura da concha de electrões de um átomo de ferro atesta a sua localização nas sub-grupos, confirma que pertence à família de Dr. elementos.

Estar na natureza
O ferro é um dos elementos químicos mais comuns que ocorrem naturalmente. Na crosta seu conteúdo percentual é de cerca de 5,1%. Em mais nas profundezas do nosso planeta, existem apenas três elementos: silício, alumínio, oxigénio.
minérios de ferro são encontrados em diferentes regiões da Terra. Alquimistas foram encontrados composto desse metal no solo. Na produção do minério de ferro é seleccionado no qual o teor for superior a 30 por cento.
O ferro magnético contém cerca de setenta e dois por cento do metal. depósitos de magnetita básicos estão localizados em Kursk anomalias magnéticas, bem como em Southern Montes Urais. Na pedra de sangue percentagem de ferro chega a 65 por cento. Hematita foi encontrado na área de Krivoy Rog.

O valor para plantas e animais
Que papel nos organismos vivos, realiza ferro? A estrutura do átomo explica as suas propriedades de restauração. Este elemento químico faz parte da hemoglobina, dando-lhe uma cor vermelha distintiva. Aproximadamente três gramas de ferro puro, a maioria dos quais é incorporado em hemoglobina, encontradas no corpo de um adulto. O objectivo principal é o de transferir para os tecidos dos pulmões do oxigénio activo e a retirada de dióxido de carbono formado.
Precisa desse metal e plantas. Como parte do citoplasma, que tem um papel activo no processo da fotossíntese. Se a planta não é suficiente ferro, suas folhas têm uma cor branca. Com sais de vestir mínimas de planta de ferro folhas ficarem verdes.
Propriedades físicas
Revisamos a estrutura do átomo de ferro. O circuito confirma que este elemento de brilho metálico (valência electrões disponíveis). Em um metal de ponto de fusão relativamente elevado de prata-branco (1539 graus Celsius). Devido à boa ductilidade do metal pode ser facilmente rolamento, estampagem, forjamento.
Capacidade de magnetização e desmagnetização característico de ferro, fez um excelente material para a produção de núcleos de eletroímãs poderosos em diferentes veículos e carros elétricos.
ferro como ativo? A estrutura mostra a presença do átomo ao nível exterior dos dois electrões que serão dadas no decurso de uma reacção química. Para aumentar a sua dureza e resistência, e executar de metal endurecido rolamento adicional. Tais processos não são acompanhadas por uma alteração na estrutura do átomo.

espécies de ferro
A estrutura electrónica do átomo de ferro, o esquema que foi discutido acima, explica as suas características químicas. Em metais comercialmente puro, que é aço de baixo teor de carbono cujo principal componente é o ferro. À medida que a impureza revelou cerca de 0,04 por cento de carbono, também contém fósforo, azoto, enxofre.
ferro quimicamente puro em seus parâmetros externos semelhantes a platina. Tem elevada resistência à processos de corrosão, estável para ácidos. Ao menor impurezas são introduzidos num metal puro suas características únicas desaparecer.
as opções para
A estrutura dos átomos de alumínio e de ferro pertencentes anfotérico indicar o principal subgrupo de alumínio, a possibilidade da sua utilização no processo de separação de ferro a partir dos seus óxidos. Aluminotermia levada a cabo a temperatura elevada, que permite identificar pura de metal a partir de minérios naturais. Além de alumínio como um agente de redução forte é seleccionado de hidrogénio, um óxido de carbono (2) e carvão.
Especialmente propriedades químicas
Quais são as propriedades químicas de ferro é? A estrutura do átomo explica a sua actividade redutora. Para o ferro, caracterizado pela formação das duas séries de compostos tendo o estado de oxidação +2, +3.
No ar húmido, há um processo de oxidação (corrosão) do metal, resultando na formação de hidróxido de ferro (3). Com oxigénio aquecida fio de ferro reage com o advento do pó de óxido de ferro negro (2.3), um chamado escala de óxido de ferro.
No metal de alta temperatura capaz de reagir com vapor de água, formando-se assim um óxido misto. O processo é acompanhado pela libertação de hidrogénio.
A reacção com não-metais ocorre apenas no aquecimento preliminar dos componentes de partida.
O ferro pode ser dissolvido em sulfúrico diluído ou ácido clorídrico, sem pré-aquecimento da mistura. sulfúrico concentrado e ácido clorídrico passivar o metal.
O que mais tem propriedades de ferro químico? A estrutura de um átomo do elemento indica a sua actividade média. Esta localização é confirmada ferro de hidrogénio (H2) na série electroquímica. Por conseguinte, pode deslocar a partir dos sais de todos os metais, que estão localizados à direita na linha Beketova. Assim, a reacção com cobre (2) é levada a cabo sob aquecimento, é uma atribuição de cobre puro e a obtenção de uma solução de cloreto férrico (2).
 aplicações
aplicações
A maior parte do ferro total é usada na produção de ferro e aço. O teor percentual de ferro de carbono de 3-4 por cento no aço – não mais do que 1,4 por cento. Este elemento metalóide executa a função de aumentar a resistência de ligação. Além disso, afecta positivamente as propriedades de corrosão de ligas aumenta a resistência do material a uma temperatura elevada.
vanádio aditivos necessários para melhorar a resistência mecânica do aço. O cromo aumenta a resistência a produtos químicos agressivos.
propriedades ferromagnéticas deste elemento químico tornou popular em aplicações industriais, incluindo nos eletroímãs. Além disso, o ferro encontrado seu uso na indústria de souvenir. A base para a produção de vários lembranças tais ímãs coloridos na geladeira.
Resistência e ductilidade permite o uso de metal para a criação de armaduras, várias armas.
O cloreto de ferro (3) usado para a purificação de água de impurezas. Na medicina 26 do elemento de tabela periódica utilizado no tratamento de doenças tais como a anemia. No caso de uma escassez de glóbulos vermelhos existe fadiga, pele olhar pele anormalmente pálida. preparações de ferro ajudar a eliminar este tipo de problema, devolver o corpo para atividades normais. O ferro tem particular importância para a actividade da glândula tiróide, do fígado. Assim que o corpo humano não é nenhum problema sério, consumir suficiente diária cerca de 20 mg do metal.













