O dióxido de cloro: aplicações de fórmula. A acção de dióxido de cloro sobre o corpo
O dióxido de cloro, ou ClO 2 – é um composto inorgânico de um elemento químico Cl (cloro) com o elemento químico O (oxigénio). Neste artigo, vamos olhar para em grande detalhe a substância e descubra onde é usado, como ele é produzido em laboratórios e indústria, uma vez que age sobre o corpo.
O que é a sílica? Ao contrário do dióxido de óxido de
Muitos estudantes estão perdidos com a visão da palavra "sílica", porque nesta ciência, como a química, este conceito é um pouco fora da data. A palavra "sílica" ainda podem ser encontrados em livros didáticos, livros e na internet, mas algumas escolas já parou para explicar o que é.
Então, todos nós sabemos que este óxido. Óxido de – um composto de oxigénio (O), com quaisquer outros produtos químicos elemento menos electronegativo. Óxido e um ClO2. Dióxido é vulgarmente chamado um composto em que está presente dois átomos de O. O prefixo "di" em "gel" significa "dois".
Se você ouve a palavra "sílica" significa, neste contexto, dois átomos de oxigênio. Isso irá ajudá-lo a escrever a fórmula química do composto.
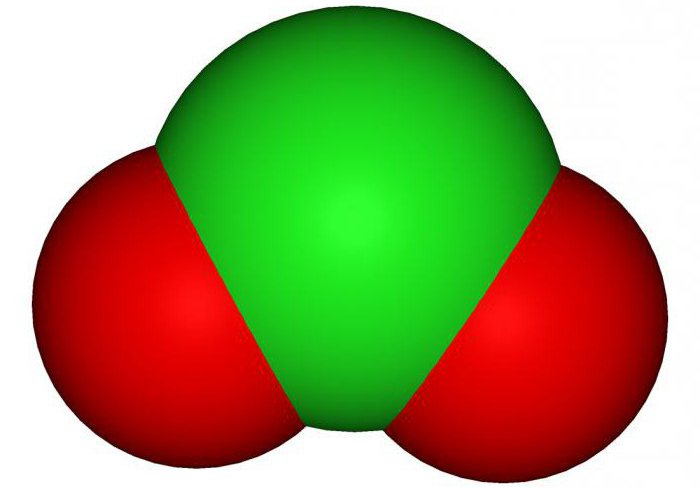
As propriedades físicas da substância
O dióxido de cloro – uma substcia gasosa que tem um odor característico, e cor de vermelho-amarelo. Mas a uma temperatura abaixo de 10 graus Celsius substância altera o seu estado físico e transforma-se num líquido castanho-avermelhado. Quando explode aquecidas. Muito bem e rapidamente se dissolve na água. Muito bem misturados e solúveis em certos solventes orgânicos, tais como ácido acético e ácido sulfúrico. temperatura de fusão é de substância -59 graus centígrados, e o seu ponto de ebulição – apenas 9,7 graus Celsius.
método laboratorial preparação
Até à data, utilizar apenas um método para a produção de dióxido de cloro no laboratório – por reacção de clorato de potássio (KClO 3) com o ácido oxálico, que tem a fórmula H 2 C 2 O 4. Como resultado desta reacção é alocado ClO 2, bem como água e de sódio oxalato.
No entanto ClO 2 pode receber uma outra maneira. Para este efeito, há uma instalação especial. Instalação de dióxido de cloro – é um modelo científico útil. Uma instalação deste tipo compreende uma unidade de controlo, um reactor para as bombas de transferência de vários reagentes para o reactor, bem como uma variedade de válvulas e as válvulas. Para ClO 2 usando ácido sulfúrico, soluções de cloreto de sódio e clorato de sódio. Isso resulta em uma solução de dióxido de cloro.

método de preparação industrial
ClO 2, os cientistas aprenderam como produzir e forma industrial. Para produzir esta reacção de redução em que o clorato de sódio é reduzido com dióxido de enxofre. Na reacção de dióxido de cloro é libertado, a preparação do qual já feita, e sulfato de hidrogénio de sódio.
As propriedades químicas da substância
Em dióxido de cloro tem várias propriedades químicas importantes. ClO 2 é um óxido ácido (que exibe propriedades ácidas, e também forma ácido kislosoderzhaschie). Após a dissolução em água de dióxido de cloro ocorre uma reacção de desproporção, isto é, a formação de tais ácidos como cloroso e clórico. Se a própria óxido de cloro explode a luz, as suas soluções são bastante estáveis no escuro e à luz não explodir, mas lentamente degradada.
ClO2 em muitas reacções se comporta como força média oksilitel, reage com muitos compostos da química orgânica.
aplicação
O dióxido de cloro, cuja utilização é bastante comum em todo o mundo, é agora o mais popular. a substância mais frequentemente atua lixívia. óxido de cloro utilizado em particular para o branqueamento de materiais, tais como papel, farinha, etc.
Além disso, a substância é considerada pelos químicos ClO 2 um dos mais poderosos agentes antimicrobianos em todo o mundo. É por isso que muitas vezes é usado para esterilização e desinfecção de materiais diversos. Ele mata micróbios patogénicos, por oxidação, devido ao facto de que o oxidante é uma média. O dióxido de cloro, que aplicação devido ao aumento nas propriedades ácidas, é agora um material indispensável.
Esta substância é insubstituível na indústria, precisamente porque existem muito poucas substâncias que desinfectar materiais econômica e ambientalmente amigável. Desinfecção com o uso de ClO 2 é absolutamente seguro para o ambiente que nos rodeia. Até hoje, o uso de gás e líquido Cl para esterilização e desinfecção. Mas nos últimos anos, devido a questões ambientais, utilizando a mais segura desinfetante – dióxido de cloro. Ao contrário de substância pura cloro, conhecido por nós ClO2 não entrar na reacção de cloração com outras substâncias e dos elementos químicos.
Água desinfectada com cloro, uma bebida pode não só, mas também a ser usado para lavar a pele. Mas dióxido de cloro tem ajudado a resolver este problema: ele é completamente seguro, porque ele não participa da reação de cloração.

A acção de dióxido de cloro sobre o corpo
O dióxido de cloro, o seu efeito sobre o organismo estudado por cientistas durante várias décadas. Agora é um produto químico amplamente utilizado na indústria alimentar como aditivo E926. Infelizmente, muitos suplementos E são muito prejudiciais, e as pessoas comuns, os consumidores de produtos, pouco se sabe sobre eles. Alguns aditivos, no entanto, são inofensivos, mas não é especialmente perigoso. O dióxido de cloro pode ser fornecida poseredinke: é prejudicial para o corpo humano, é indesejável, mas o produto químico não tem efeitos secundários graves sobre o corpo humano, ao contrário do popular glutamato de sódio hoje.
Quando a utilização de aditivos alimentares disso, você pode receber uma tosse, às vezes bastante forte e de longa duração, irritação das mucosas, ataques de asma. Após contacto com a substância para as vias aéreas dos pulmões pode ocorrer irritação.

O dióxido de cloro – É uma coisa muito interessante que os cientistas estudam tem sido por muitos séculos. Ele é insubstituível na indústria, especialmente em alimentos, é ambientalmente amigável e seguro (é claro, só se usado corretamente).