ligação química – é um conceito bastante complexo, que foi formado um longo tempo com base nos ensinamentos e idéias sobre a estrutura do átomo. Assim, nos séculos XVI -XVII foram as primeiras tentativas de explicar a semelhança química baseada na doutrina corpuscular. Boyle pensou que a força de condução de reacções químicas, é a coincidência de partículas do tipo de chave de bloqueio, t. E. Os átomos são "ir" e "compreendido", para formar novas substâncias. Mais tarde, no século XVIII. substituir a teoria mecânica vem dinâmico, que era um defensor de Newton. Ele acreditava que a causa da semelhança química é a força de atração de intensidade diferente. 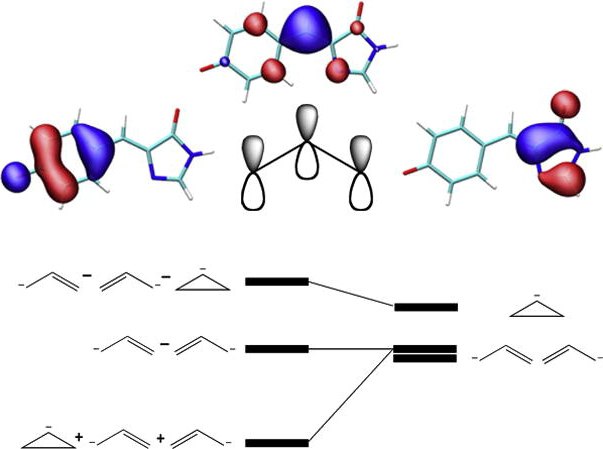 No século XIX. Começa período eletroquímica. Neste momento, um químico alemão Kekulé sugeriu que a valência é igual ao número de átomos de ligações químicas. Usando esta afirmação aço representam fórmulas de estrutura das moléculas em que traços designadas ligações químicas. Era todos os pré-requisitos para a explicação do conceito de "comunicação química", que está completamente formada apenas após a descoberta do electrão. Se a hipótese de que depois de que as substâncias são formadas pelo movimento ou mudança de electrões de um átomo para outro. Ao longo do tempo, esta suposição foi confirmada científica e agora é usada, afirmando que uma ligação química é formada através da interacção de electrões e os núcleos dos átomos que fazem parte das moléculas.
No século XIX. Começa período eletroquímica. Neste momento, um químico alemão Kekulé sugeriu que a valência é igual ao número de átomos de ligações químicas. Usando esta afirmação aço representam fórmulas de estrutura das moléculas em que traços designadas ligações químicas. Era todos os pré-requisitos para a explicação do conceito de "comunicação química", que está completamente formada apenas após a descoberta do electrão. Se a hipótese de que depois de que as substâncias são formadas pelo movimento ou mudança de electrões de um átomo para outro. Ao longo do tempo, esta suposição foi confirmada científica e agora é usada, afirmando que uma ligação química é formada através da interacção de electrões e os núcleos dos átomos que fazem parte das moléculas.
Explicar a natureza das comunicações electrónicas vai ajudar um átomo de hidrogênio. Sabe-se que ela contém um electrão não emparelhado, que é o primeiro nível de energia. Quando dois átomos de hidrogénio de um deles começa a atrair electrões núcleo do outro, e vice-versa. átomos Mezhuyev interacção ocorre, a distância entre eles diminui, a atracção mútua é equilibrada pela repulsão dos núcleos. A molécula, que acabou de se formar, a densidade de electrões é aumentada. 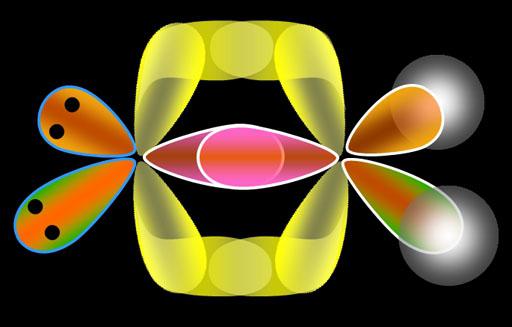 Estas duas nuvens de electrões partículas elementares são combinados para formar uma nuvem electrónica molécula. Simplificando, a ligação química é o resultado da sobreposição de orbitais de electrões de átomos diferentes, devido à interacção de electrões desemparelhados.
Estas duas nuvens de electrões partículas elementares são combinados para formar uma nuvem electrónica molécula. Simplificando, a ligação química é o resultado da sobreposição de orbitais de electrões de átomos diferentes, devido à interacção de electrões desemparelhados.
No entanto, nem todos os átomos de interagir. Assim, não se sobrepõem as conchas de electrões de gases inertes, isto é, que permanecem estáveis. Com base nesta regra formulado octetos de Lewis, o que indica que todos os átomos de elementos de formação de ligação química tendem a alterar a configuração do escudo electrónico mais próximo do gás inerte, ou por fixação que dão electrões.
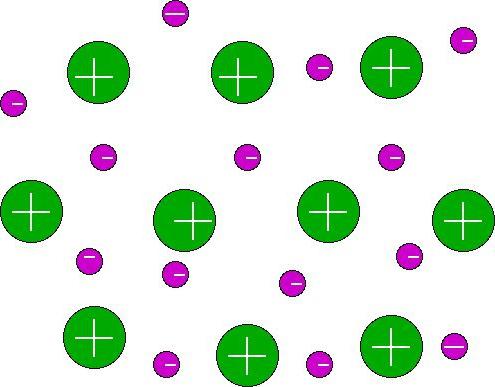 Substâncias existentes são vários tipos de comunicação. Assim, não há iônica, metálica, covalente, doador-receptor. Por exemplo, a ligação química de metais existe apenas em elementos metálicos. Ele é formado pelo recuo de electrões 1-2 cada átomo, isto é, partículas adjacentes são "dividido" electrões, que formam um tipo de gelatina. Nesse ambiente os íons metálicos estão localizados.
Substâncias existentes são vários tipos de comunicação. Assim, não há iônica, metálica, covalente, doador-receptor. Por exemplo, a ligação química de metais existe apenas em elementos metálicos. Ele é formado pelo recuo de electrões 1-2 cada átomo, isto é, partículas adjacentes são "dividido" electrões, que formam um tipo de gelatina. Nesse ambiente os íons metálicos estão localizados.
Com base no acima exposto, pode-se concluir que a ligação química é uma interacção entre átomos, que ocorre por meio da troca de electrões ou uma transição a partir de uma das partículas elementares de material para outro.