tiocianato de potássio – uma substância tóxica usada em química analítica
tiocianato de potássio (em moderno nomenclatura IUPAC – tiocianato de potássio) – cristais sem cor e odor; em branco adquirir finamente dividido. A substância tem um pungente sabor amargo, é venenoso. tiocianato de potássio é altamente solúvel em muitos solventes, tais como água, etanol, e álcool amílico.
recepção
O composto foi preparado somente por meios químicos, distingue-o a partir de fontes naturais (no sangue e saliva de pessoas) – é extremamente caro. De modo a sintetizar o tiocianato de potássio, necessários para misturar soluções de tiocianato de amónio e hidróxido de potássio (nome comum – hidróxido de potássio).
O experimento foi realizado sob uma cobertura, porque o amoníaco pode causar queimaduras químicas e envenenamento; em seguida, filtração da solução purificada foi evaporado e o resíduo para dar cristais da substância desejada. Quando o produto de saída a setenta por cento e amostra pura tiocianato de amónio suficiente, este método é muito eficaz.

Outra maneira é enxofre ligado com cianeto de potássio, mas um tal processo para a preparação de tiocianato de potássio é bastante perigoso devido à elevada toxicidade do cianeto.
aplicação
tiocianato de potássio aplicável, os seus derivados, e as soluções com diferentes concentrações de alguns sectores. Por exemplo:
- indústria têxtil.
- filme fotográfico.
- síntese orgânica.
- química analítica.
Áreas de utilização

- Na indústria têxtil. solução de tiocianato de potássio é utilizado para condicionar tecidos, por exemplo – de seda, durante a aplicação e manuseamento para preservar as propriedades iniciais de material.
- Na síntese orgânica. A partir de tiocianato de potássio sintetizado algumas substâncias orgânicas, tais como tioureia, um óleo de mostarda sintéticos e vários corantes. Também se obteve com a ajuda de outros tiocianatos, por exemplo, – cobre tiocianato-2.
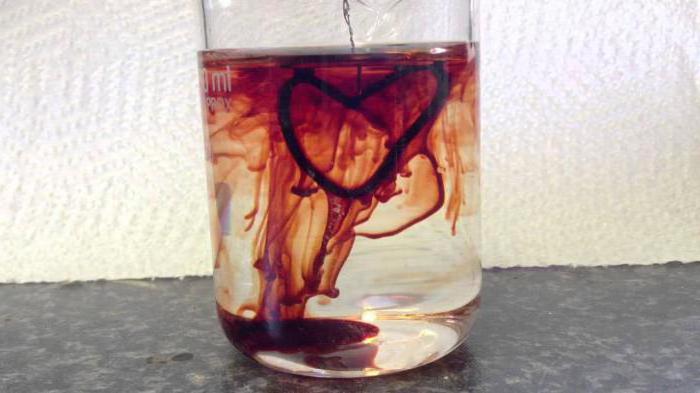
- Em química analítica, solução de tiocianato de potássio é utilizado para a determinação de catiões de ferro trivalente no material. Um exemplo ilustrativo é o de reacção, o qual envolve de tiocianato de potássio e cloreto férrico-3, também chamado de "sangue de água", em que um hexacianoferrato de potássio púrpura-vermelho 3; nome comum – sal vermelho sangue. Tiocianatos, também usado para a separação de metais raros, tais como tório e lantânio. Tiocianato, cloreto de potássio e geleia ajuda ultimamente na produção de sangue artificial para kinosomok, mas este método vai no esquecimento devido à introdução na produção do filme de computação gráfica.
- Na agricultura, a partir de soluções obtidas tiocianatos insecticidas fortes. Há duas reações possíveis:
- Primeiro – receber tiociano gás por exclusão sal de potássio; Rodan é um gás muito perigoso para todos os organismos vivos e é raramente utilizado.
- Segunda – dissolução de tiocianato de potássio, a carga libertada durante ácido tsianovodorodnoy hidrólise e oxidação da substância resultante de cianogénio. Ciano – não menos tóxicos, mas mais gás pesado em comparação com Rodan, e, portanto, muitas vezes é utilizado como um insecticida.
tiocianato de potássio é uma substância tóxica a dose letal é de cerca de 0,9 gramas de substância por kg de peso corporal na preparação oral do composto.
disponibilidade
tiocianato de potássio pode ser comprado em qualquer loja de produtos químicos, mas em pequenas quantidades, devido à bastante elevada toxicidade. O preço médio de um reagente – quatro rublos por quilograma, vendendo principalmente limitado a duas libras por pessoa.
segurança
Devido à sua toxicidade, tiocianato de potássio deve ser armazenado em condições especiais de acordo com os regulamentos de segurança para a manipulação de substâncias tóxicas:
- Os cristais e as soluções de tiocianato de potássio proibida ingerida e penetração altamente indesejável de soluções com uma elevada concentração da substância de base para a pele.
- Apesar do fato de que a droga é tóxica somente quando aplicar obra interior com a substância é desejável no revestimento de borracha luvas de laboratório, e, como com todos os produtos químicos sobre os requisitos básicos de segurança.
- É necessário isolar o material de crianças e pessoas que não têm conhecimento do técnico, pois pode causar incidentes desagradáveis com a perda de reagentes, mau uso, e morte súbita.
- Desde substância não inflamável e suficientemente estável no ar, é possível administrar a substância de armazenamento no escuro. armário seco. Evitar a alta humidade e a luz solar directa, como pode acontecer devido a deterioração do reagente de decomposição das suas partes componentes. Também NFPA 704 rotulagem ortorrômbica padrão tem os seguintes símbolos: 3 0 0 W, em que 3 (um losango azul) – toxicidade, 0 (para o vermelho e amarelo) – inflamabilidade e reactividade, e W – marca para a interacção com água, que é libertado ácido tiociânico venenoso.

E lembre-se, experimentos químicos – é incrível e única, mas nunca negligenciar as precauções de segurança!