O que é IAD em química moderna?
Vamos falar sobre o que o ISI na síntese orgânica e inorgânica.
definição do processo
Sob reacções redox envolve processos tais como um resultado do qual vai mudar o estado de oxidação de dois ou mais elementos químicos em substâncias simples ou complexos.

O que é a oxidação
Por esses meios a oxidação da reacção química, processo esse em que um átomo ou ião específico perde electrões, diminuindo assim o seu número de oxidação inicial. Este processo é característica de metais.
Qual é a recuperação
No âmbito do processo de recuperação envolve uma transformação química, resultando no grau de oxidação vai diminuir o ião ou uma substância simples, a adição de electrões ocorre. Esta reacção é característica de não-metais e resíduos ácidos.
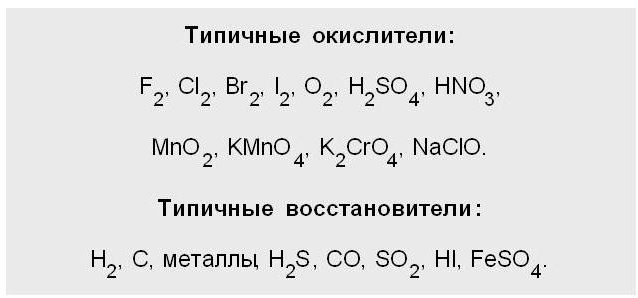
Característica redutor
Considerando a questão do que é iAd, não podemos ignorar tal coisa como um "agente redutor".
Ele refere-se a uma molécula neutra ou iónica carregada, que como um resultado de interacção química de iões irão favorecer a outro átomo ou electrões, aumentando assim o seu grau de oxidação.
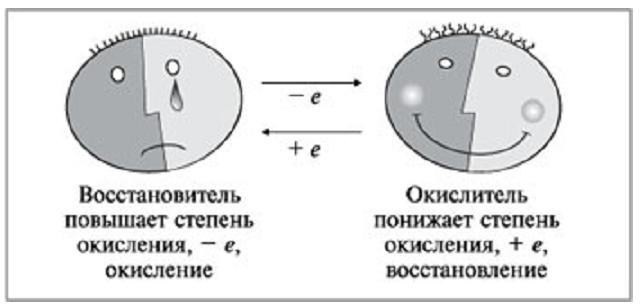
Determinação de oxidante
Raciocínio sobre o que OVR também é importante mencionar um termo como "oxidante". Sob que são tomadas para significar iões ou átomos neutros que por interacção química terá electrões negativos de outros átomos ou partículas neutras. Ao mesmo tempo, seu estado de oxidação originais irá diminuir.
tipos ISI
Discutindo sobre o iAd, deve-se notar sobre as variedades destes processos, que são muitas vezes consideradas na síntese orgânica e inorgânica.
interacções intermoleculares envolvem tais processos em que os átomos e um agente oxidante e agente redutor estão localizados em diferentes substâncias de partida, que se faz reagir. Como um exemplo deste tipo de transformação pode resultar em interacção entre o óxido de manganês (4) e uma solução de ácido clorídrico em que o gás de cloro é formado, cloreto manganoso e água.
Neste processo químico aniões como redutoras de oxidação aparecem como cloro interacção. catião manganês (com oxidação 4) exerce capacidade da reacção de oxidação, aceitar dois electrões, é reduzida.
interacção intramolecular é de transformações químicas, tais, como um agente redutor e que os átomos e oxidante são inicialmente átomos uma substância de partida, e depois a conversão eles estão nos vários produtos da reacção.
Como um exemplo deste tipo de reacção pode ser representada por uma decomposição de clorato de potássio. Depois de se aquecer a substância vai ser convertido ao cloreto de potássio e oxigénio. propriedades oxidativas são característicos do anião de clorato, o que, tendo cinco electrões na reacção irá recuperar transformado em cloreto.
Neste caso, o anião oxigénio irá exibir propriedades de redução, são oxidados para oxigénio molecular. Então, qual é o IAD neste caso? Este processo de transferência de electrões entre os iões, que conduz à formação dos dois produtos da reacção.
Também para este tipo de reacções químicas que ocorrem com a mudança em estados de oxidação elementos estão inicialmente num fórmula processo de decomposição de nitrito de amónio refere-se. Azoto em pé no catião amónio tendo o estado de oxidação três, durante o processo envia uma seis electrões e é oxidado a azoto molecular. E o azoto, o qual é um membro de nitrito, recebe seis electrões, com um agente redutor, e durante a reacção é oxidado.
O que é iAd em química? Definição considerado acima mostra que esta transformação associada com alterações em vários elementos de oxidação.
A auto-oxidação e recuperação (disparidade) assume tais processos no decurso da qual como agente redutor e o agente oxidante serve um átomo de partida que irá aumentar e, simultaneamente, reduzir o seu estado de oxidação após a conclusão da reacção. Discutindo sobre o iAd é em química, exemplos de tais transformações pode ser encontrado até mesmo no curso de química do ensino médio. sulfito de decomposição de potássio mediante aquecimento resulta na formação de dois sais de metais: sulfeto e sulfato. O enxofre no estado de oxidação +4 e propriedades de redução de oxidação e exibe por levantar e baixar os indicadores de estado de oxidação.
Para entender o que isso significa WRA na química, que chamamos de uma outra forma de tais transformações químicas. Kontrproportsionirovanie envolve processos tais como um resultado de que o oxidante e átomos redutoras são compostos por vários componentes de partida, mas no lado direito, que formam um produto de reacção. Por exemplo, por reacção de um óxido de enxofre (4) com sulfureto de hidrogénio para formar enxofre e água. De iões de enxofre no estado de oxidação 4 terá quatro electrões, e o ião de enxofre com indicador -2 perde dois electrões. Como um resultado, ambos eles são transformados em uma substância simples, que tem um estado de oxidação igual a zero.

conclusão
Considerando a questão do que é ISI em química, notamos que esta conversão múltipla, pelo qual os organismos vivos função, coloque uma variedade de processos e fenômenos naturais. A fim de organizar as equações em tais fatores, é necessário fazer uma balança eletrônica.