tabela periódica de Mendeleev e lei periódica
Durante o século XIX uma reforma forte sofrido muitas áreas, incluindo a química. Sistema Periódico Mendeleev, formulado em 1869, tem levado a um entendimento comum da relação entre a posição de substâncias simples na tabela periódica, para estabelecer a relação entre a propriedade de massa e elemento de valência atómica relativa.
química Domendeleevsky entre
Um pouco mais cedo, no início do século XIX, inúmeras tentativas de sistematização de elementos químicos. O químico alemão Johann Wolfgang Döbereiner passou o primeiro trabalho sério sobre a sistematização no campo da química. Ele determinou que uma série de substâncias semelhantes nas propriedades podem ser agrupados – tríade.
Imprecisão das representações do cientista alemão
A essência da lei representado por Johann Wolfgang Döbereiner tríades determinada de modo que o peso atômico de uma substância está perto de metade da soma das massas atômicas dos dois últimos elementos da tabela tríades (valor médio). 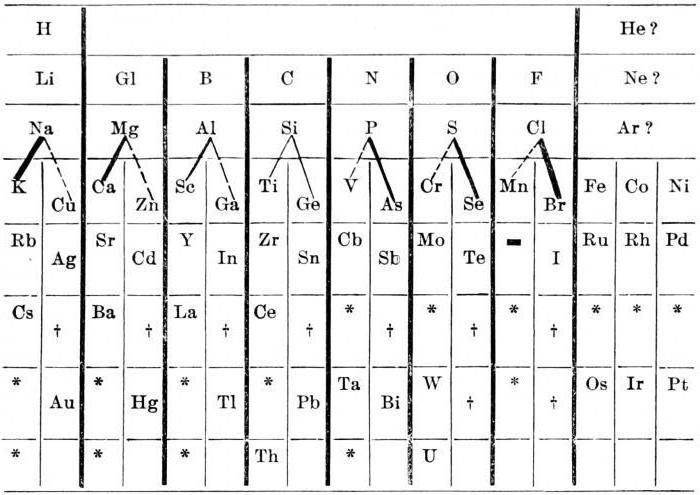 No entanto, a ausência de magnésio em um único subgrupo de cálcio, estrôncio e bário estava errada.
No entanto, a ausência de magnésio em um único subgrupo de cálcio, estrôncio e bário estava errada.
Esta abordagem foi a consequência das limitações artificiais substâncias semelhantes apenas triodidades. Johann Wolfgang Döbereiner podia ver as semelhanças entre parâmetros químicos de fósforo e arsênico, bismuto e antimônio. No entanto, ele limitou-se Recuperar tríades. Como resultado, ele foi incapaz de chegar à classificação correcta dos elementos químicos.
Em Elementos existentes, em Johann Wolfgang Döbereiner tríade, é claro, não foi possível, a lei indicado claramente a presença da relação entre a massa atómica relativa e propriedades químicas de substâncias simples.
elementos químicos processo sistematização
Todas as tentativas subseqüentes para sistematizar contou com a distribuição dos elementos de acordo com a sua massa atômica. Mais tarde Johann Wolfgang Döbereiner hipótese tem sido usado por outros químicos. Introduzido formando tríades, e tetradas pêntadas (combinando em grupos de três, quatro e cinco elementos).
Na segunda metade do século XIX houve várias obras simultaneamente, com base no qual Dmitri Ivanovich Mendeleev química levou à sistematização completa de elementos químicos. estrutura diferente da tabela periódica levou a um entendimento revolucionário e evidência de mecanismo de distribuição de substâncias simples.
tabela periódica de Mendeleev de elementos
Em uma reunião do russo Chemical Society, na primavera de 1869 foi lido um aviso no cientista russo D. I. Mendeleeva sobre sua descoberta da lei periódica de elementos químicos.  No final do mesmo ano, a primeira obra "Fundamentos da Química", o primeiro sistema periódica dos elementos incluídos nele foram publicados.
No final do mesmo ano, a primeira obra "Fundamentos da Química", o primeiro sistema periódica dos elementos incluídos nele foram publicados.
Em novembro de 1870, ele mostrou colegas disso, "sistema natural dos elementos e usá-lo na direção das qualidades dos elementos desconhecidos." Neste trabalho D. I. Mendeleev usado pela primeira vez o termo "lei periódica". O sistema periódico de elementos com base na lei periódica define a possível existência de substâncias simples não abrir e indica claramente as suas propriedades.
Correções e esclarecimentos
Como resultado, em 1971, a lei periódica e do sistema periódico de elementos de Mendeleyev foram modificados e complementados pelo químico russo.
O artigo final "lei periódica de elementos químicos" definição do conjunto de cientista da lei periódica, o que indica que as características dos organismos simples, as propriedades dos compostos, e formam corpos complexos dependência directa são determinados de acordo com o seu peso atómico.
Um pouco mais tarde, em 1872, a estrutura da tabela periódica foi reorganizado em uma forma clássica (o modo de curto período de distribuição). 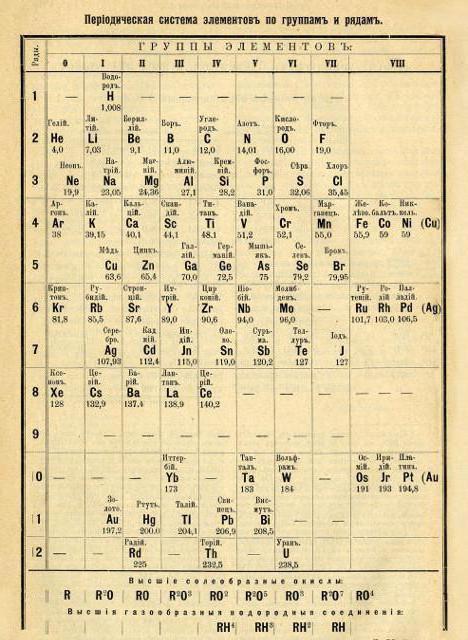
Ao contrário de seus antecessores, o químico russo plenamente a mesa, introduziu o conceito de regularidade dos pesos atômicos dos elementos químicos.
Elementos característicos da tabela periódica e as leis derivados permitiram aos cientistas para descrever as propriedades dos elementos ainda para ser descoberto. Mendeleev baseou-se no facto de que as propriedades de cada substância pode ser determinada de acordo com as características dos dois elementos adjacentes. Chamou-o a regra das "estrelas". A sua essência é que os elementos químicos na tabela para determinar as propriedades do elemento seleccionado necessário ser guiado horizontalmente e verticalmente em uma tabela de elementos químicos.
periódica de Mendeleev é capaz de prever o …
Tabela dos elementos Mendeleev, apesar de sua precisão e fidelidade, não foi reconhecido pela comunidade científica totalmente. Alguns dos grandes cientistas de renome mundial ridicularizado abertamente a possibilidade de prever as propriedades dos elementos desconhecidos. Foi somente em 1885, depois da descoberta dos elementos previstos – EKA-alumínio, e ekabora ekasilitsiya (gálio, escândio e germânio), um novo sistema de classificação de lei periódica de Mendeleev e têm sido reconhecidos como os fundamentos teóricos da química.
No início do século vinte, a estrutura da tabela periódica repetidamente corrigido. No processo de obtenção de novos dados científicos D. I. Mendeleev e seu colega William Ramsay chegou à conclusão sobre a necessidade de introduzir um grupo zero. Na sua composição inclui gases raros (hélio, néon, árgon, crípton, xénon e rádon).
Em mil novecentos e onze anos Soddy fez uma proposta para colocar elementos químicos indistinguíveis – isótopos – em uma única célula da tabela.
No curso de um trabalho longo e árduo da tabela periódica dos elementos químicos da tabela periódica foi finalizado, e adquiriu uma aparência moderna. A sua estrutura inclui oito grupos e sete períodos. Grupos – são períodos colunas verticais – horizontal. Os grupos definidos divisão em subgrupos. 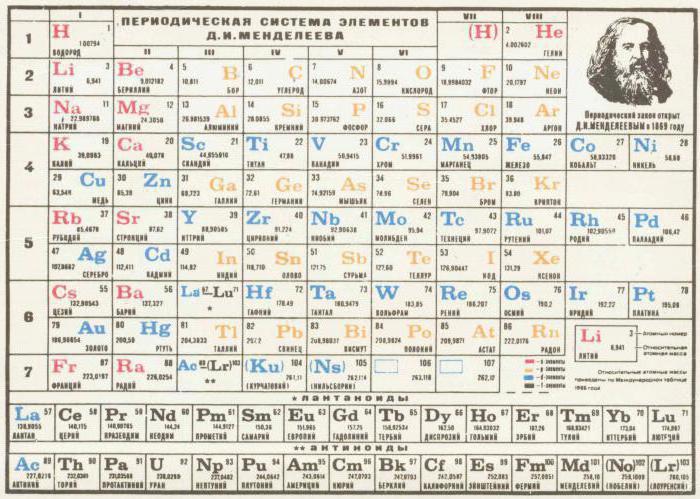
A posição do elemento de quadro indica os seus electrões de valência e características puramente químicos. Como se verificou, durante o desenvolvimento da tabela periódica que foi detectada uma coincidência o número de elementos de electrão com o seu número de série.  Este fato é simplificada ainda mais a compreensão do princípio da interação de substâncias simples ea formação de complexo. Um processo como no sentido inverso. O cálculo do número de este material, bem como necessário para a reacção química era teoricamente disponível.
Este fato é simplificada ainda mais a compreensão do princípio da interação de substâncias simples ea formação de complexo. Um processo como no sentido inverso. O cálculo do número de este material, bem como necessário para a reacção química era teoricamente disponível.
O papel da descoberta da ciência moderna de Mendeleev
sistema de Mendeleev e sua abordagem para a ordenação dos elementos químicos determinou o desenvolvimento sensível da química. Com a compreensão adequada da relação das constantes e análises químicas Mendeleev poderia montar corretamente e elementos agrupados de acordo com suas propriedades.  Nova tabela de elementos faz com que seja possível calcular com clareza e precisão os dados antes para a reacção química, a previsão de novos elementos e as suas propriedades.
Nova tabela de elementos faz com que seja possível calcular com clareza e precisão os dados antes para a reacção química, a previsão de novos elementos e as suas propriedades.
Abertura do cientista russo teve um impacto direto sobre o novo ciclo de desenvolvimento da ciência e tecnologia. Não há nenhuma área tecnológica que não seria envolvido conhecimento de química. Talvez, se tal descoberta não aconteceu, nossa civilização teria tomado um caminho diferente de desenvolvimento.