Em química inorgânica moderna classificação e as propriedades dos elementos de interacção e os seus sais de todos os possíveis compostos de grande importância. Existem substâncias que, entre outros ocupam um lugar especial. Tais compostos, em particular, deve ser referido sulfato de cálcio. Fórmula substância CaSO4.
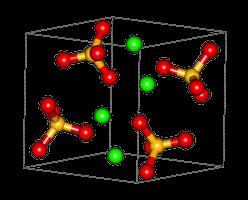 Relativamente grandes depósitos deste composto em crosta permitir o seu uso como matéria-prima na preparação de materiais diferentes. Os materiais resultantes podem ser usados com sucesso na construção, medicina e outras áreas.
Relativamente grandes depósitos deste composto em crosta permitir o seu uso como matéria-prima na preparação de materiais diferentes. Os materiais resultantes podem ser usados com sucesso na construção, medicina e outras áreas.
depósitos minerais encontrados com uma composição de CaSO4 2 H2O em condições naturais. sulfato de cálcio também é encontrado no mar (cerca de 1800 000 toneladas por metro cúbico) e de água fresca.
CaSO4 anidrido é uma densidade de pó branco de 2,90-2,99 gramas por centímetro cúbico. Composto ativamente absorve a humidade do ar. Devido a esta propriedade, e sulfato de cálcio utilizado como o agente de secagem.
Em temperaturas mil quatrocentos e cinquenta derrete graus de substâncias e decompõe. A solubilidade da substância é aumentada na presença de HCl, HNO3, NaCl, MgCl2. sulfato de cálcio reage com o ácido sulfúrico é reduzida quando a sinterização com carbono.
Estar na água juntamente com MgSO4 e MgCl2, CaSO4 rigidez dá-lhe uma constante. fluido química amaciadora é possível com os reagentes. Redução da dureza da água com base na introdução de substâncias enriquecido seus aniões.
 Abrandamento da água é também efectuada por permuta iónica. Este método baseia-se na capacidade de determinados permutadores de iões sintéticos e naturais – compostos de elevado peso molecular – radicais trocando incluído em sua composição, sobre os iões presentes na solução. Como permutadores de iões aluminossilicatos actuam frequentemente (Na2 [Al2Si2O8] ∙ nH2O, por exemplo).
Abrandamento da água é também efectuada por permuta iónica. Este método baseia-se na capacidade de determinados permutadores de iões sintéticos e naturais – compostos de elevado peso molecular – radicais trocando incluído em sua composição, sobre os iões presentes na solução. Como permutadores de iões aluminossilicatos actuam frequentemente (Na2 [Al2Si2O8] ∙ nH2O, por exemplo).
Hidratar com a composição 2CaSO4 H2O – Alabaster (gesso queimado) – utilizados no fabrico de materiais de cimento. Estas substâncias representam um compostos pulverulentos, de que, quando misturado com água forma plástica em primeiro lugar, e, subsequentemente solidificar em um peso de corpo sólido. processo de preparação é levado a cabo na calcinação de gesso alabastro sob a influência da temperatura de cento e cinquenta a cem setenta graus. Esta propriedade é utilizada no fabrico de painéis de separação e placas, moldes de itens, bem como na aplicação de reboco.
 Calcinação sob a influência da temperatura de mais de duas centenas de graus conduz à formação da forma solúvel de anidro sulfato de cálcio, a uma temperatura superior a cinco centenas de graus – forma insolúvel. O último perde a sua capacidade de fixar a água, por conseguinte, não pode ser usado como um ligante.
Calcinação sob a influência da temperatura de mais de duas centenas de graus conduz à formação da forma solúvel de anidro sulfato de cálcio, a uma temperatura superior a cinco centenas de graus – forma insolúvel. O último perde a sua capacidade de fixar a água, por conseguinte, não pode ser usado como um ligante.
gesso natural pode ser utilizado como um material de partida na preparação de cimento e ácido sulfúrico pelo método combinado.
sulfato de cálcio natural também pode ser utilizado como um dessecante para a análise de compostos orgânicos. O composto anidro é capaz de absorver a humidade de 6,6% do peso total. O sulfato de cálcio é também utilizado no fabrico de materiais isolantes.