Talvez, cada casa tem uma cozinha refrigerante – caixa de aparência comum com uma substância em pó. Anfitriã culinário usá-lo como um aditivo para as preparações de cozimento. No entanto, o seu âmbito é tão ampla que uma substância pode seguramente ser chamado de assistente universal pessoa. Mas o que é um refrigerante? Que tipo e como ele existe é usado na vida cotidiana?

nomes de refrigerante
Antes de prosseguir para as propriedades químicas de sódio, vale a pena mencionar que o seu nome – "Soda", uma substância obtida a partir do nome da planta saltwort sodonosnaya, cinzas, que é uma fonte de produção de soda.
Em química, soda – que generaliza sais de sódio do título de ácido carbónico:
- Na 2 CO 3 (carbonato de sódio) – fórmula química do carbonato de sódio;
- Na 2 CO 3 · 10H 2 O – carbonato de sódio;
- NaHCO3 – bicarbonato de sódio. Esta é a fórmula química de bicarbonato de sódio;
- Na 2 CO 3? H 2 O ou de Na 2 CO 3? 7H 2 O – fórmula química cristal de sódio.
Na vida cotidiana, assim como existem vários tipos de material trivial na indústria química:
- bicarbonato de sódio;
- bicarbonato de sódio;
- bicarbonato de sódio;
- aditivo E500;
- deca-hidrato de sódio.

A fórmula empírica
A fórmula química de bicarbonato de sódio – de NaHCO 3. Este ácida de sal de ácido carbónico. Se você somar os pesos atômicos de todos os seus elementos constitutivos, verifica-se o peso atômico do sódio é igual a 84 a. e.
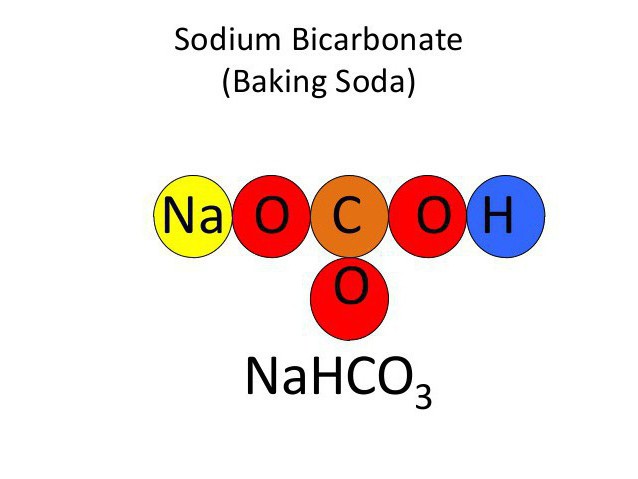
O método de sua formação é bastante simples. A fórmula química de bicarbonato de sódio – uma interacção complexa de hidróxido de sódio com ácido carbónico:
NaOH + H 2 CO 3 = NaHCO3 + H2O
Em química, sódio dvuuglikisly é um complexo de hidrogénio de sódio anião carbonato e de catiões. Ao introduzir estes elementos no corpo, eles normalizar o equilíbrio ácido-base ao neutralizar o excesso de ácido presente no meio líquido.
carbonato de sódio
A fórmula química do carbonato de sódio – Na2CO3. Carbonato de sódio – é um material branco, granular, que pode ser representado na forma de peletes (A) ou de pó (B).
Este tipo de cinzas tem várias características que distinguem o carbonato de sódio dos alimentos.
- pH do meio. E alimentos e carbonato de sódio – é alcalino, mas o primeiro – de baixo, com pH = 8, e a segunda – alta, com um pH = 11. A natureza do meio e a fórmula química indica refrigerante técnica.
- Scope. Bicarbonato de sódio é usado na culinária, cosméticos e medicamentos. Sódio é usado como um agente de limpeza eficaz.
No uso doméstico utilizando o carbonato de sódio pode ser:
- envolvido em lavagem, usando-o como um detergente para a roupa;
- lavar o chão, mas esta ferramenta não é adequado para laminados e soalhos, uma vez que podem estragar o revestimento;
- remover bloqueios de tubo;
- artigos de porcelana limpo.
Quando se utiliza o carbonato de sódio deve ser muito cuidadoso, desde substância altamente tóxico relacionado com este terceiro grupo de agentes perigosos.

As propriedades físicas de bicarbonato de sódio
O bicarbonato de sódio é uma substância em pó branca. Este complexo elementos sódio, hidrogénio, carbono e oxigénio.
Por densidade do pó igual a 2,16 g / cm 3.

Quando o parâmetro de temperatura de 50 -60 C. substância começa a derreter.
bicarbonato de sódio, ou bicarbonato de sódio é representado sob a forma de leite em pó. No ambiente aquático perfeitamente solúvel. Ele não queima. A fórmula química de bicarbonato de sódio é a mesma que a dos alimentos.
solução de soda

Bicarbonato de sódio – uma substância que se dissolve completamente em água, resultando numa solução de soda. Ele é usado para fins de higiene como um bochecho.
solução fórmula química de sódio é como se segue:
De NaHCO 3 + H 2 O = H 2 CO 3 + NaOH.
A solução de soda aquosa dotado carácter fracamente básico.
De sódio dissocia-se dvuuglikisly em solução aquosa de modo a formar os iões seguintes:
Na 2 CO 3 ↔ 2Na + + CO3 2-
Propriedades de sódio como um alcali
Como já foi mencionado, o carbonato de hidrogénio de sódio é uma substância alcalina. Este fato afeta o uso de bicarbonato de sódio como um meio para neutralizar a acidez do corpo, especialmente o estômago. Os elementos que compõem a matéria, têm uma exposição segura.
operabilidade de sódio renal melhora porque derivável urina tem um meio alcalino. Além disso, mantém a quantidade necessária de AK glutâmico no corpo, o que evita o aparecimento de formações de pedra nos rins.
ambiente alcalino ajuda a uma melhor digestão de certas vitaminas do complexo B: B1, B4, B5, B6 e B12.
Quando refrigerante usado para uma boa digestão combiná-lo com leite quente. Isto contribui para o facto de que o pequeno intestino de sódio reage com os aminoácidos de leite, o que poderia resultar em sal de sódio de aminoácidos possuindo uma natureza alcalina. Estes aminoácidos são muito melhores do que a soda, entrar na corrente sanguínea, aumentando deste modo as reservas alcalinas do corpo.
soda cáustica
A fórmula química de soda cáustica – NaOH. fórmula estrutural: Na – O – H.
As substâncias de peso molecular constituem o peso atómico dos seus componentes constituintes de Na, S e H. É igual a 40.
Cáustica perfeitamente solúvel em água.
Na indústria em relação a este tipo de refrigerante são utilizados os seguintes nomes:
- soda cáustica;
- hidróxido de sódio;
- hidróxido de sódio.
Ao trabalhar com a soda cáustica é necessário o uso de itens de proteção de roupa, como em contacto com a pele deixa queimaduras graves.
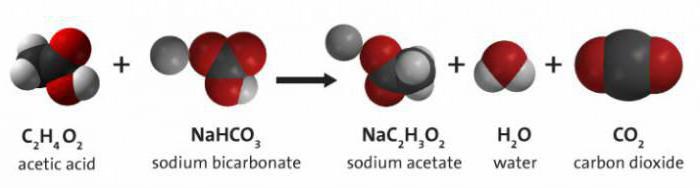
Refrigerante em combinação com vinagre
fórmula química vinagre e bicarbonato de sódio é uma reacção de têmpera que a água produzida, o dióxido de carbono e o sal de ácido acético.
Este produto químico "experiência" vem acompanhada de um silvo característico, o que indica o início da soda "queima".
Esta reacção efectua-se no negócio culinário, quando destinados a amassar a massa para assar. Vinagre para isso é levado a uma concentração de 9%. análogo do ácido pode ser um suco de limão, maçã cidra ou vinagre de vinho.
Então, por efectuar a reacção na preparação do teste? A única coisa que é resultante da decomposição de dióxido de carbono de sódio dá esplendor teste.
substância recebendo
Depois extraiu-se a partir de carbonato de sódio plantas halophytes sodonosnoy. Actualmente a base para a preparação desta substância é uma forma natural de sulfato de sódio. Preparação de reacção é como se segue, em que o lado direito é exibida fórmula química sódio:
Na 2 SO 4 + 3C + 2O 2 = 2Na 2 CO 3 + CO 2 + 2SO 2;
CaCO3 + C + Na 2 SO 4 = Na 2 CO 3 + 4CO + CaS.
O uso de bicarbonato de sódio
Soda é muito popular na vida cotidiana, não só como um componente culinária. Mas um olhar mais atento a casos em que a cinza é usado.
- Para começar é de mencionar uma vez que a soda – componente alimentar no negócio culinário. A sua utilização não é aleatória: por aquecimento do composto capaz de libertar vapores de dióxido de carbono, que por sua vez dá leveza teste. Neste caso refrigerante atua como um agente de desintegração. Mas se você comprar em um saco de armazenamento com massa de fermento em pó, em seguida, sobre o pacote na linha pode detectar a presença de refrigerante, que é designado como um aditivo alimentar E500.
- Use bicarbonato de sódio e bebidas carbonatadas.
- Muitas vezes, soda é usado na chamada medicina "folclórica". Nesta região, a mesma sobressai cura refrigerante quase quaisquer doenças, por exemplo, a sua eficácia tem sido provado para a azia, tosse, dor de garganta, o estômago, a uma temperatura elevada.
- bem e bicarbonato de sódio realizado como um agente de limpeza. Ele pode ser usado para a limpeza de sanitários, panelas de alumínio, pratos, tapetes, de prata e de lavandaria. A substância tem um bom desinfectante e anti-fúngico.
- Muitas mulheres usar bicarbonato de sódio para fins cosméticos e de higiene. Ele pode ser usado como um esfoliante para a pele. Meios bela defesa da pele áspera pés, se usado para banhos de pé. Ele pode ser usado para se livrar do cheiro de suor na área das axilas, ou no sapato.
Ele ajuda os dentes de refrigerante e de branqueamento. Esta é uma maneira barata, mas eficaz. refrigerante em pó é misturada com pasta de dentes e água ou movimentos suaves realizadas a limpeza dos dentes.
soda cáustica: uso
Usando este tipo de refrigerante deve ser acompanhada de certas medidas de segurança como a soda cáustica – um forte alcalino que podem "comer fora" muitos tipos de superfícies.
O que também pode ser útil em termos domésticos cáusticos?
- Cáustica lida com diferentes impurezas sobre os pratos. Mas é necessário que se abstenha do uso deste agente para produtos feitos de alumínio e Teflon. Mas para o resto dos potes, panelas ou tabuleiros – por favor. Nagar, escala, camadas entupido de gordura – tudo isso é fácil de manusear cáusticos.
- A soda cáustica pode resolver o problema de canos entupidos. Você só precisa preencher a substância granular no tubo e deixe por um tempo, em seguida, enxaguar com água corrente.
A soda cáustica, também conhecido como soda cáustica, é amplamente aplicável a uma escala industrial em vários campos de produção.
- Em construção. Aqui, a substância usada para fazer alguns tipos de materiais de construção, e também serve como um componente adicional que reforça a base fundamental das estruturas.
- Na indústria de alimentos. A soda cáustica é aplicável e alimentos de fabricação. É claro que, neste caso, é utilizado em baixas concentrações. Com sua participação produzir cacau em pó, chocolate, sorvete, caramelo, em cozer pão, ele é usado como um aditivo E524.
- indústria têxtil. Nesta área, a soda cáustica é útil no branqueamento de tecidos e de regeneração de produtos de borracha.
- produção de substâncias químicas: soda cáustica é usado como neutralizadores de ácidos, meios para óleo e produtos com base em que a limpeza. Produção de óleos industriais também não pode fazer sem a adição de soda cáustica. Além disso, o hidróxido de sódio – um bom catalisador de algumas reacções químicas.
- soda cáustica adequada para fazer sabão e o fabrico de vários tipos de sabões, champôs e geles.
carbonato de sódio: uso
O carbonato de sódio é também chamado de linho. demanda especial para esta facilidade apreciado na União Soviética, portanto, podemos dizer: refrigerante lavandaria é testada pelo tempo.
Os meios utilizados nas seguintes situações:
- Durante os itens de lavagem.
- Quando a limpeza das superfícies dos azulejos, faiança, louça de barro.
- Quando você remove um bloqueio nos tubos.
- Para eliminar a espuma no interior do tambor de uma máquina de lavar roupa, bem como sobre os pratos.
- Para a destruição de pragas de insectos em jardins.
A partir do exposto, a conclusão sugere-se: ferramenta versátil Soda usado na maioria das áreas de tanto a vida doméstica e industrial.
O material de boa qualidade é o fato de que você pode comprá-lo por meros tostões.