O que é luminol? Como luminol em casa
Algumas substâncias, que tomam parte em reacções químicas, têm a capacidade de emitir luz. Cada químico amador vez fabricado o líquido brilhante. Este artigo será discutido que é o luminol, como cozinhar em casa.
O que é quimiluminescência?
Muitas reações em química ocorrer com a liberação de energia. Na maioria dos experimentos, a energia é liberada na forma de calor. Na reacção de soluções alcalinas e ácidas foram aquecidas. Há casos em que a energia pode se manifestar na forma de corrente elétrica (experimentos com células eletroquímicas). Na energia combustão dos reagentes é convertida em calor e luz.
Mas há reações em que a emissão de luz ocorre, mas não há aumento da temperatura. Este fenômeno é chamado quimiluminescência. O exemplo mais gritante – frio fósforo brilho. Deve notar-se que na maioria dos reacções químicas libertar "luz fria" oxidado compostos orgânicos. Oxidantes actuam geralmente de oxigénio ou peróxido de hidrogénio.
Na natureza, há muitas substâncias que emitem luz. Mas a maior parte do brilho obtido é muito fraco e pode ser detectado apenas com equipamento especial.
Para a quimioluminescência brilhante e bonita capaz de um grupo relativamente pequeno de compostos orgânicos e inorgânicos. Nos exemplos, os seguintes materiais: luminol, siloxi, lofin, e lyutsegenin difeniloksalat. 
O que é luminol?
Luminol foi sintetizado na Alemanha em 1902, mas seu nome verdadeiro era tarde. É um cristal branco ou amarelo claro em cor, facilmente solúvel em solventes orgânicos polares. Na água, luminol é completamente insolúvel.
Esta matéria orgânica é capaz de libertar luz quando combinada com peróxido de hidrogénio ou outros oxidantes. No caso de líquidos neutros e ligeiramente ácidos, sob a luz UV, que fluoresce luz azul-claro. Em soluções alcalinas (peróxido de hidrogénio), em que a reacção prossegue na presença de catalisadores de – um composto de fósforo, sais de metais de hemina e de hemoglobina – luminescência obtidos mais saturado e brilhante.
O processo consiste em duas etapas. Ácido é aquecido com hidrazina em um solvente orgânico com um ponto de ebulição elevado (3-etileno-glicol). A condensação do sistema heterocíclico é obtida 5-nitroftalilgidrazida. Este composto é reduzido utilizando sulfureto de amónio, pelo que o formado e luminol. As mãos que podem ser preparados no laboratório de síntese de ácido 3-nitro-ftálico. 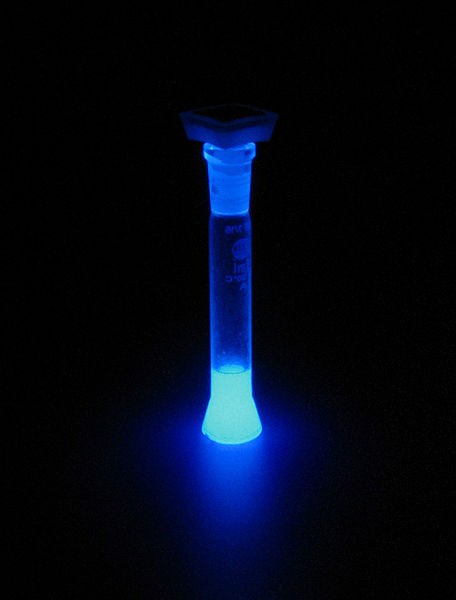
Onde o uso de luminol
A substância em questão é reage notáveis com o ferro, o qual é parte de hemoglobina. Por conseguinte, ele é amplamente utilizado em peritos forenses na identificação de vestígios de sangue e impressões digitais deixadas no local. Luminol é usado cientistas durante vários pesquisa biológica para a detecção de ferro, cobre e cianeto. 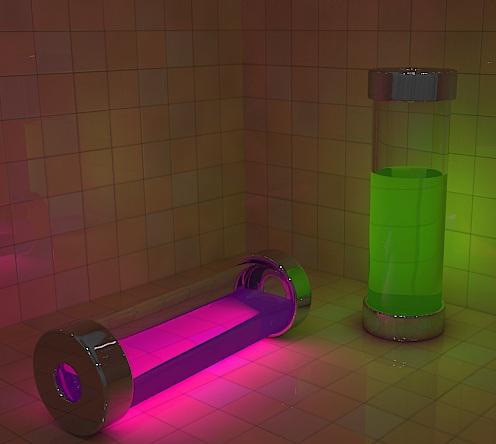
Onde comprar solução de luminol
custo luminol é bastante elevada. É possível olhar para os fóruns químicos, bases especiais ou em farmácias. Se você não sabe para onde levar o luminol, você pode comprar na farmácia "Galavit", que está disponível em comprimidos, cápsulas e supositórios. Um comprimido contém 25 mg do sal de sódio do luminol. A 50 ml de uma solução 1%, deve ser de 20 comprimidos (embalagem). Os comprimidos são moídos em pó e em seguida é adicionada água a ela. 
O peróxido de hidrogénio líquido luminosa
Há receitas para líquido brilhante improvisados. Mas para solução melhor usado luminol, porque dá uma luz azulada suave e macia. Antes de começar, certifique-se de proteger as áreas expostas do tecido denso do corpo, e nas mãos, usar luvas.
Prepare luminol em casa no (primeiro) receita clássica:
- Luminol – 2-3 gramas.
- Água – 0,1 litros.
- Uma solução de peróxido de hidrogénio (3%) – 0,08 litros.
- A soda cáustica – 0,01 litros.
- Bluestone – 3 gramas.
- Corantes (rublos, brilhante verde ou qualquer outro).
- Material de vidro (frascos ou frascos).
preparação:
- Verter em um recipiente de vidro e adicionando água luminol. misturar completamente os cristais em água, de modo que maximize-dissolvido.
- À solução resultante foi adicionado peróxido de hidrogénio.
- A composição resultante a adição de sulfato de cobre. Sulfato podem ser substituídos com cloreto férrico ou sangue sal.
- A composição mais recente para anexar soda cáustica.
- Na sala de desligar a luz. A composição resultante deve emitir uma luz azul brilhante. Se uma cor diferente, em seguida, adicionando à solução do corante fluorescente apropriado.
Segunda opção:
- solução luminol (3%) – 5 ml.
- Gidroperit (3%) – 10 ml.
- Detergente com água – 20 ml.
- permanganato de potássio.
- Qualquer jarra de vidro ou pote.
Etapas de trabalho:
- O recipiente despeje soluções luminol, pó detergente e peróxido de hidrogénio.
- Esfregar suavemente as alguns cristais de permanganato de potássio e adicioná-lo à composição total.
- Para ver o que o luminol e como ele irá se manifestar suas propriedades, desligar a luz na sala. O líquido irá emitir um brilho bonito. Se a solução é agitada periodicamente, a espuma espumante é exibida na superfície das mesmas.

Preparação da solução com sulfóxido de dimetilo
forma de realização mais interessante vai luminol oxidação pelo oxigénio atmosférico em meio Dimexidum. Luminescência ocorre na interface entre a secção de ar e da água.
precisamos preparar a composição:
- Luminol – 0,15 gramas.
- Dimexidum (DMSO) – 30 ml.
- soda cáustica a seco – 35 gramas.
- Qualquer corante fluorescente.
- Alta copos.
fases:
- Completamente misturados num balão dimexide, luminol e alcalino.
- O recipiente foi selado hermeticamente com uma tampa.
- Na sala de desligar a luz.
- O balão é levemente agitada para obter um brilho azulado. Para alterar a cor para adicionar um corante fluorescente.
- Se o brilho perdeu o seu brilho, é possível abrir o recipiente. Na admissão de ar para dentro do frasco a solução de novo torna-se brilhante e saturada.
Dicas de cozinha
Muitos alcalino na solução não é recomendado para adicionar, porque é muito difícil para dissolver e transforma o líquido em um mingau grosso. A suspensão de Dimexidum luminol e alcalino pode ser armazenado por um longo tempo. Ao adicionar um brilho oxidante será uniforme. A sua duração depende do número e gidroperita luminol e pode chegar a 40 minutos. Mas a partir de um excesso de brilho luminol é cada vez mais fraca.
Deve notar-se que o brilho luminescência e duração também vai depender da concentração de luminol. soluções altamente diluídas dar um brilho fraco, mas muito tempo. A grande concentração de material forma uma forte brilho de toda a solução. cor da luz pode variar de azul para verde. Em formulações ricas contendo uma maior concentração de sais de sangue obtidas brilho verde. 
É possível substituir luminol?
Há situações em que é necessário para preparar o líquido luminosa sem luminol. Para fazer isso, tomar o ácido bórico e algumas gotas de fluoresceína. Estas substâncias são necessárias para misturar e aquecer a placa de metal. Líquido irão brilhar no escuro por cerca de um minuto.
Para entender o que é o luminol, melhor tentar obtê-lo a si mesmo. Como diz o ditado, melhor ver uma vez do que ouvir uma centena de vezes. Mas não se esqueça que quaisquer experiências envolvem interação com substâncias corrosivas e prejudiciais. Por isso, é necessário observar as precauções de segurança.