De silício e os seus compostos. Silicon na natureza. O uso de silício
Um dos mais populares na arte e na indústria de elementos é o silício. Que deve suas propriedades incomuns. Hoje em dia existem muitos compostos diferentes de este elemento, que desempenham um papel importante na síntese e criação de produtos técnicos, artigos de vidro, vidro, equipamentos, materiais de construção, jóias e outras indústrias.

Características gerais de silício
Se considerarmos a posição de silicone no sistema periódico, é possível dizer:
- IV está localizada nos principais subgrupos do grupo.
- O número de sequência 14.
- massa atômica 28,086.
- O símbolo químico Si.
- Nome – silício, ou em latim – silício.
- A configuração electrónica do 4e camada exterior: 2e: 8e.
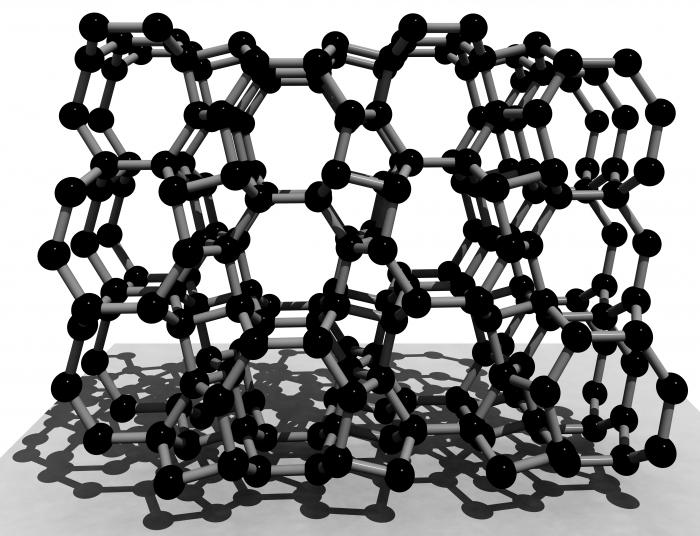
A estrutura de cristal de silício é semelhante à estrutura de diamante. Os nós são átomos dispostas, o seu tipo – uma face centrada cúbico. No entanto, devido ao maior comprimento das propriedades físicas de comunicação de silício diferem fortemente das propriedades de modificação alotrópica de carbono.
Propriedades físicas e químicas
Existem dois modificação alotrópica do elemento: amorfa e cristalina. Eles são muito semelhantes. No entanto, como é o caso de outros materiais, a principal diferença entre eles – o reticulado de silício cristalino.
Neste caso, ambas as versões – um pó de cores diferentes.
1. silício cristalino é uma cinza de metal em pó como negro brilhante. A sua estrutura corresponde à do diamante, mas propriedades diferentes. Ele tem:
- fragilidade;
- baixa dureza;
- Propriedades semicondutores;
- A temperatura de fusão de 1415 0 C;
- densidade 2,33 g / cm 3;
- a temperatura de ebulição de 2700 0 C.
A sua actividade química é baixa em comparação com outra forma alotrópica.
2. O silício amorfo – pó de cor castanha, tem a estrutura diamante silnorazuporyadochennogo. Reatividade é alta o suficiente.
Em geral, deve-se notar que reagem não gosta de silício. Para fazê-lo reagir, temperatura necessária não inferior a 400-500 0 C. Vários compostos químicos são formados de silício sob estas condições. Tais como:
- óxidos;
- halogenetos;
- suicídios;
- nitretos;
- boretos;
- carbonetos.
Talvez a interacção de silício com ácido nítrico ou um alcalino, o que é chamado um processo de ataque químico. silicones generalizada, que agora estão se tornando mais comuns.
Estar na natureza
O silício é encontrado naturalmente em uma quantidade bastante significativa. Ele está em segundo lugar depois de prevalência de oxigênio. A sua fracção de peso é de cerca de 30%. A água do mar também contém um elemento activo numa concentração de 3 mg / L. Portanto, não podemos dizer que o silício na natureza – é um elemento raro.
Pelo contrário, há muitas rochas e minerais diferentes, como parte do que ocorre e do qual pode ser extraído. Os compostos de silício naturais mais comuns são:
- Sílica. A fórmula química de SiO 2. Há uma grande variedade de formas de minerais e rochas em sua base: areia, pedra, feldspato, quartzo, cristal de rocha, ametista, calcedônia, cornalina, opala, Jasper e outros.
- Silicatos e silicatos de alumínio. Caulino, feldspato, mica, sais de ácido silícico, amianto, talco.
Assim, a propagação amplamente em silício natureza e seus compostos são populares e a demanda para as pessoas usarem para fins técnicos.

Silício e seus compostos
Desde puro considerar que existe elemento não pode, portanto, têm importância diferente dos seus compostos. Do ponto de vista químico, pode ser três estado de oxidação +2, 4, -4. Partindo desta, e também por causa da sua inércia, mas especialmente para a estrutura de rede cristalina, que gera os seguintes principais tipos de substâncias:
- compostos binários com elementos não-metálicos (silano, carboneto, nitreto, fosforeto, e assim por diante;
- óxidos;
- ácido silícico;
- silicatos de metal.
Vamos considerar o quão importante o silício e seus compostos, são os mais comuns e popular para as pessoas.

óxidos de silício
Existem dois tipos de substâncias expressas pela fórmula:
- SiO;
- SiO2.
No entanto, o mais utilizado tem dióxido. Ela existe na natureza sob a forma de um belíssimo pedras semi-preciosas:
- ágata;
- calcedônia;
- opala;
- cornalina;
- jaspe;
- ametista;
- strass.
O uso de silício nesta forma encontrou aplicação na fabricação de jóias. Incrivelmente bela ouro e jóias de prata feito com essas semi-preciosas e pedras semi-preciosas.
Algumas variações da sílica:
- quartzo;
- rio e areia de quartzo ;
- pederneira;
- feldspatos.
O uso de silicone em tais tipos implementadas na construção civil, engenharia, eletrônica, indústria química, metalurgia. Juntos, os óxidos listados referem-se a uma única substância – sílica.
Karbid Kremniya e seu uso
Silício e seus compostos – um material do futuro e o presente. Um tal material é o carboneto de silício ou carboneto do elemento. A fórmula química do SiC. Ela ocorre na natureza como o moissanite mineral.
Em forma pura de carbono e o composto de silício – é bonito, cristais transparentes, estrutura semelhante a diamante. No entanto, para fins técnicos utilizados pintado em material de cor verde e preto.
Principais características da substância, permitindo seu uso na indústria, tecnologia, indústria química, o seguinte:
- ampla semicondutor lacuna;
- muito alta resistência (7 na escala de Mohs) ;
- resistente a altas temperaturas;
- excelente elektroustoychivost e condutividade térmica.
Tudo isto permite a utilização de carboneto de silício como um material abrasivo em síntese química e metalurgia. LEDs também, se baseia produzir um largo espectro de acção, peças para forno de vidro, bicos, tochas, jóias (moissanite apreciado FIANITE acima).

Silano e seu significado
composto de silício é hidrogénio silano e o nome não pode ser obtido por síntese directa a partir de materiais de partida. Para obter a vários metais silicietos são usados, os quais são submetidos a um tratamento ácido. Como resultado, o gás de silano é libertada e forma um sal de metal.
É interessante que o composto em questão nunca produziu sozinho. Sempre na reacção de uma mistura de mono-, di- e trisilano em que os átomos de silício estão ligados entre si em cadeias.
Sobre as propriedades destes compostos – agentes de redução forte. -Se, portanto, facilmente oxidado pelo oxigênio, às vezes de forma explosiva. violenta reação com halogênios sempre com um monte de liberação de energia.
A aplicação dos seguintes silanos:
- Reacções de síntese orgânica, como um resultado de que é importante para os silicones – de silicone, borracha, selantes, lubrificantes, emulsões e outros.
- Microelectronics (monitores de LCD, diagramas técnicos integrados, etc).
- Alta pureza polissilício.
- próteses dentárias.
Assim, os silanos no mundo moderno é alta.

ácido silícico e silicatos
Hidróxido do elemento – eles são diferentes sílicas. destacam-se:
- meta;
- o;
- polissilício e outros ácidos.
Todos eles têm características comuns – o extremo desequilíbrio no estado livre. Eles são facilmente decomposto pelo calor. Sob condições normais, não são de curta duração, transformando em primeiro lugar num sol e, em seguida, um gel. Após secagem, os géis de sílica, tais estruturas são chamadas. Eles são utilizados como adsorventes em filtros.
Importante do ponto de vista da indústria, são os sais de ácidos silícicos – silicatos. Elas são a base da preparação de tais substâncias, tais como:
- vidro;
- concreto;
- cimento;
- zeólito;
- caulim;
- porcelana;
- barro;
- cristal;
- cerâmica.
silicatos de metais alcalinos solúveis, – o resto – NO. Portanto, o silicato de sódio e de potássio é chamado vidro de água. adesiva papelaria normal – isto é o sal de sódio de ácido silícico.
Mas os compostos mais interessantes são todos do mesmo copo. Qual únicas opções para essa substância nenhuma idéia! Hoje, dada coloridas, ópticas, opções de mate. Vidraria é surpreendente em seu esplendor e diversidade. Quando a adição de certos metais e óxidos de metalóide para a mistura pode obter uma grande variedade de tipos de vidro. Por vezes, mesmo a mesma composição, mas diferentes percentagens de componentes conduz a uma diferença nas propriedades da substância. Exemplos são porcelana e louça, cuja fórmula de SiO 2 Al 2 O * 3 * K 2 O.
De vidro de quartzo – é uma forma de produto de alta pureza, cuja composição é descrita como sílica.

na descoberta de compostos de silício
Ao longo dos últimos anos, estudos têm mostrado que o silício e seus compostos – os participantes mais importantes do estado normal de organismos vivos. C deficiência ou o excesso de um determinado elemento de doenças associadas, tais como:
- câncer;
- tuberculose;
- artrite;
- cataratas;
- lepra;
- disenteria;
- reumatismo;
- hepatite e outras.
processos de envelhecimento-se também estão associados com o teor quantitativo de silício. Numerosas experiências sobre os mamíferos têm mostrado que a ausência de um vírus elemento ter ataques cardíacos, acidentes vasculares cerebrais, cancro e hepatite C é activado.