Aplicação de etileno. Propriedades de etileno
O etileno é o mais simples dos compostos orgânicos conhecidos como alcenos. É um gás inflamável incolor que tem um gosto e cheiro suaves. As fontes naturais incluem gás natural e óleo, é também um hormônio natural nas plantas em que inibe o crescimento e promove o amadurecimento dos frutos. O uso de etileno é um fenômeno comum na química orgânica industrial. É produzido por aquecimento de gás natural, o ponto de fusão é 169,4 ° C, com ebulição – 103, 9 ° C.
Etileno: características estruturais e propriedades
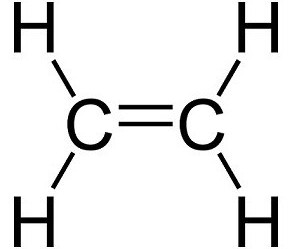
Os hidrocarbonetos são moléculas que contêm hidrogênio e carbono. Eles variam muito em termos de número de ligações simples e duplas e a orientação estrutural de cada componente. Um dos hidrocarbonetos mais simples, mas biologicamente e economicamente vantajosos é o etileno. É fornecido em forma gasosa, é incolor e inflamável. Consiste em dois átomos de carbono de ligação dupla com átomos de hidrogênio. A fórmula química tem a forma C 2 H 4 . A forma estrutural da molécula é linear devido à presença de uma ligação dupla no centro.
O etileno possui um odor amargo e almíscar que facilita a identificação de uma substância no ar. Isto aplica-se ao gás na forma pura: o cheiro pode desaparecer quando misturado com outros produtos químicos.
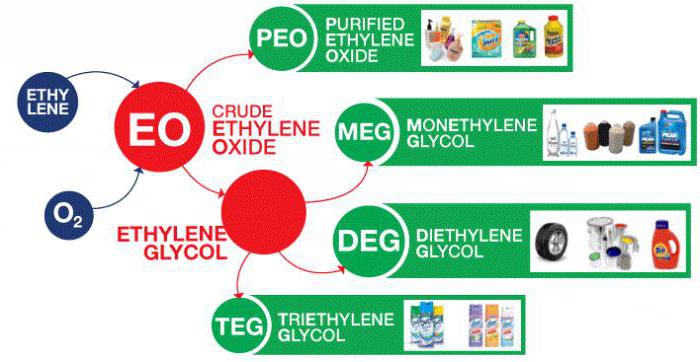
O esquema de aplicação de etileno
O etileno é usado em duas categorias principais: como um monómero a partir do qual são construídas grandes cadeias de carbono e como material de partida para outros compostos de dois carbonos. As polimerizações são associações recorrentes de muitas pequenas moléculas de etileno em grandes. Este processo ocorre em altas pressões e temperaturas. Os campos de aplicação do etileno são numerosos. O polietileno é um polímero que é usado especialmente massivamente na produção de filmes de embalagem, revestimentos de arame e garrafas plásticas. Outra utilização de etileno como monómero diz respeito à formação de a-olefinas lineares. O etileno é o material de partida para a preparação de vários compostos de dois carbonos, tais como etanol (álcool técnico), óxido de etileno (anticongelante, fibras e filmes de poliéster ), acetaldeído e cloreto de vinilo. Além destes compostos, o etileno com benzeno forma etilbenzeno, que é utilizado na produção de plásticos e borracha sintética. Esta substância é um dos hidrocarbonetos mais simples. No entanto, as propriedades do etileno tornam-se biologicamente e economicamente significativas.
Uso comercial
As propriedades do etileno proporcionam uma boa base comercial para uma grande quantidade de materiais orgânicos (contendo carbono e contendo hidrogênio). Moléculas únicas de etileno podem ser unidas para produzir polietileno (o que significa muitas moléculas de etileno). O polietileno é utilizado para a fabricação de plásticos. Além disso, pode ser usado para fabricação de detergentes e lubrificantes sintéticos, que são produtos químicos usados para reduzir a fricção. O uso de etileno para produzir estireno é importante no processo de criação de borracha e embalagem protetora. Além disso, é usado na indústria de calçados, especialmente no que se refere aos calçados esportivos, bem como na produção de pneus de automóveis. O uso de etileno é comercialmente importante e o próprio gás é um dos hidrocarbonetos mais produzidos em escala global.
Perigo para a saúde
O etileno apresenta um risco para a saúde principalmente porque é altamente inflamável e explosivo. Também pode atuar como droga em baixas concentrações, causando náuseas, tonturas, dores de cabeça e perda de coordenação do movimento. Em concentrações mais elevadas, atua como anestésico, causando perda de consciência, insensibilidade à dor e outros irritantes. Todos esses aspectos negativos podem ser motivo de preocupação principalmente para as pessoas que trabalham diretamente com o gás. A quantidade de etileno que a maioria das pessoas encontra na vida cotidiana geralmente é relativamente pequena.
Reações de etileno
1) Oxidação. Esta é a adição de oxigênio, por exemplo, na oxidação de etileno em óxido de etileno. É utilizado na produção de etilenoglicol (1,2-etanodiol), que é utilizado como líquido não congelante e na produção de poliésteres por meio de polimerização por condensação.
2) Halogenação – reações com etileno de flúor, cloro, bromo, iodo.
3) Cloração de etileno na forma de 1,2-dicloroetano e posterior conversão de 1,2-dicloroetano em monómero de cloreto de vinilo. O 1,2-dicloroetano é um solvente orgânico útil e também é um precursor valioso na síntese de cloreto de vinilo.  4) A alquilação é a adição de hidrocarbonetos sobre uma ligação dupla, por exemplo, a síntese de etilbenzeno a partir de etileno e benzeno, seguida de conversão em estireno. O etilbenzeno é um intermediário para a produção de estireno, um dos monómeros de vinilo mais utilizados. O estireno é um monómero utilizado para a produção de poliestireno.
4) A alquilação é a adição de hidrocarbonetos sobre uma ligação dupla, por exemplo, a síntese de etilbenzeno a partir de etileno e benzeno, seguida de conversão em estireno. O etilbenzeno é um intermediário para a produção de estireno, um dos monómeros de vinilo mais utilizados. O estireno é um monómero utilizado para a produção de poliestireno.
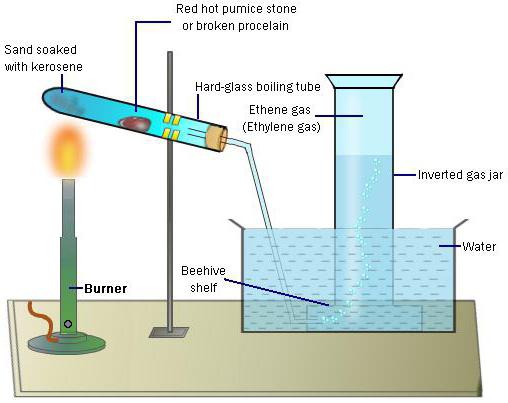
5) Combustão de etileno. O gás é obtido por aquecimento de álcool etílico e ácido sulfúrico concentrado.
6) A hidratação é uma reação com a adição de água a uma ligação dupla. A aplicação industrial mais importante desta reação é a conversão de etileno em etanol.
Etileno e combustão
O etileno é um gás sem cor, que é pouco solúvel em água. A combustão de etileno no ar é acompanhada pela formação de dióxido de carbono e água. Em forma pura , o gás queima com uma chama de difusão de luz. Misturado com uma pequena quantidade de ar, dá uma chama composta por três camadas separadas – um núcleo interno – gás não queimado, uma camada azul-verde e um cone externo, onde um produto parcialmente oxidado de uma camada pré-misturada queima em uma chama de difusão. A chama resultante mostra uma série complexa de reações e, se for adicionado mais ar à mistura de gases, a camada de difusão desaparece gradualmente.
Fatos úteis
1) O etileno é um hormônio natural das plantas, que afeta o crescimento, desenvolvimento, maturação e envelhecimento de todas as plantas.
2) O gás não é prejudicial e não é tóxico para os seres humanos em uma determinada concentração (100-150 mg).
3) É usado em medicina como anestésico.
4) O efeito do etileno diminui a baixas temperaturas.
5) Uma propriedade característica é um bom poder de penetração através da maioria das substâncias, por exemplo, através de caixas de embalagem de papelão, paredes de madeira e até mesmo de concreto.
6) Embora seja inestimável devido à sua capacidade de iniciar o processo de maturação, também pode ser muito prejudicial para muitas frutas, vegetais, flores e plantas, acelerando o processo de envelhecimento e reduzindo a qualidade do produto e sua vida útil. O grau de dano depende da concentração, duração da exposição e temperatura.
7) O etileno é explosivo em altas concentrações.
8) O etileno é utilizado na produção de vidro de propósito especial para a indústria automotiva.
9) Fabricação de estruturas metálicas: o gás é usado como gás oxigênio-combustível para corte de metal, soldagem e alta velocidade de pulverização térmica.
10) Refinação: o etileno é usado como refrigerante, especialmente na liquefação de gás natural.
11) Como mencionado anteriormente, o etileno é uma substância muito reativa, além disso, também se acende muito facilmente. Por razões de segurança, geralmente é transportado por um gasoduto separado especial.
12) Um dos produtos mais comuns feitos diretamente do etileno é plástico.