A fim de estabelecer a composição qualitativa de muitos alimentos utilizados reacção ksantoproteinovaya para a proteína. A presença de aminoácidos aromáticos na mistura irá mudar de uma cor da amostra de teste positivo.
O que é a proteína
É também chamado de uma proteína, que é um material de construção para o corpo vivo. Proteínas manter o tamanho do músculo, restaurar as estruturas de tecidos feridos e mortos de vários órgãos, seja cabelo, pele e ligamentos. Com a sua participação, produz glóbulos vermelhos do sangue, é regido pelo funcionamento normal de muitos hormônios e células do sistema imunológico. 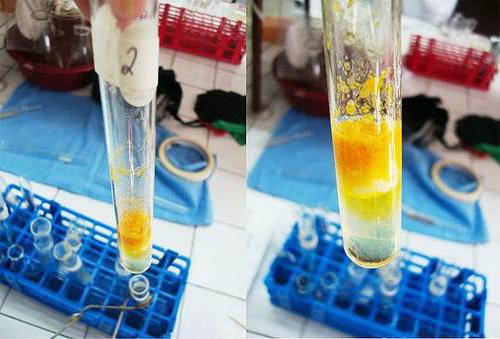
Esta é uma molécula complexa que é um polipéptido que tem uma massa maior do que 6 ~ 10 3 daltons. estrutura de proteína formando resíduos de aminoácidos em um grande número de ligao acoplado a um péptido.
A estrutura das proteínas
A característica distintiva destas substâncias em comparação com péptidos de baixo peso molecular é de que eles desenvolveram uma estrutura espacial tridimensional, efeitos com diferentes graus de atracção suportado. As proteínas possuem quatro-estrutura. Para cada um deles tem suas próprias características.
Como a base do principal organização das moléculas derivadas sequência de aminoácidos, estrutura que reconhece reacção ksantoproteinovaya para a proteína. Esta estrutura é uma repetição periódica ligação peptídica -HN-CH-CO-, um radicais parte selectivos são as cadeias laterais de aminoácidos. Eles definem outras propriedades da substância, como um todo.
A estrutura proteica primária é considerado forte o suficiente, isto é devido à presença de fortes interacções covalentes em ligações peptídicas. A formação de níveis subsequentes ocorre dependendo dos atributos definidos na fase inicial.
A formação da estrutura secundária é possível devido à torção da sequência de aminoácidos em uma espiral, em que ligações de hidrogénio são estabelecidas entre as voltas.
organização nível terciário de moléculas formadas pela aplicação de uma de uma espiral sobre os outros fragmentos com a ocorrência de todas as ligações possíveis entre eles, com hidrogénio, dissulfureto, covalente ou composto iónico. O resultado é a associação sob a forma de glóbulos. 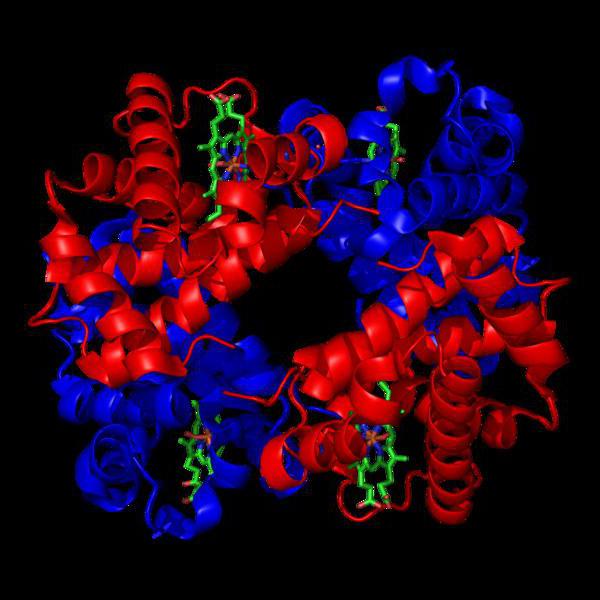
O arranjo espacial das estruturas terciias com a formação de ligações químicas entre os leva para a formação da forma final da molécula ou níveis quaternário.
aminoácidos
Eles causam as propriedades químicas das proteínas. Há cerca de 20 principais aminoácidos que compõem os polipéptidos numa sequência diferente. Este ácido aminocarboxílico raro é também referido na forma de hidroxiprolina e hidroxilisina derivado de péptido básico.
Como sinal de reacção proteína ksantoproteinovaya reconhecimento, a presença de certos aminoácidos fornece a mudança de cor de reagentes, o que sugere a presença de estruturas específicas na sua composição.
Como se verificou, são ácidos carboxílicos que ocorreram substituição do átomo de hidrogénio no grupo amino.
Um exemplo de estrutura da molécula podem servir uma fórmula estrutural glicina (HNH- HCH- COOH) como o aminoácido mais simples. 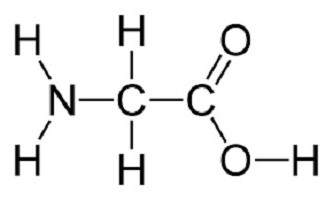
Neste caso um dos átomos de hidrogénio CH 2 – pode ser substituído por um radical de carbono mais longa, compreendendo um anel de benzeno, amino, sulfo, carboxi.
O que faz reação ksantoproteinovaya
Para a análise qualitativa de proteínas, utilizando várias técnicas. Estas incluem reacções:
- biureto com o aparecimento de cor violeta;
- ninidrina de modo a formar uma solução azul-violeta;
- formaldeído com o estabelecimento de uma cor vermelha;
- Nogier para precipitar a cor cinzenta-preta.
Na realização de cada método mostrou a presença de proteínas e a presença de certos grupos funcionais na sua molécula.
Há ksantoproteinovaya reacção com a proteína. É também chamado a repartição Mulder. Ele refere-se às reacções de coloração para proteínas, em que não são aminoácidos aromáticos e heterocíclicos.
Uma característica de um tal processo amostra é nitração nítrico ácido resíduos de aminoácido cíclico, em particular, a adesão do grupo nitro para o anel de benzeno.
O resultado deste processo é a formação de compostos nitro, que precipitaram. Esta é a reacção básica característica ksantoproteinovaya.
O que determinado o aminoácido
Nem todos ido aminocarboxico pode ser detectada utilizando uma amostra tal. A principal característica da reacção de detecção proteína ksantoproteinovaya – a presença do anel de benzeno ou um anel heterocíclico nos aminoácidos da molécula.
Uma vez que a proteína é isolada a partir de ácidos aminocarboxílicos duas aromáticos, em que há um grupo fenilo (para fenilalanina), e um radical hidroxi (em tirosina). 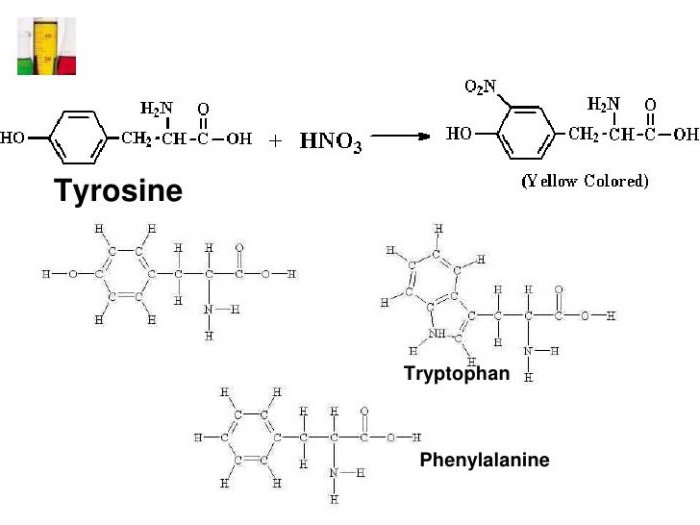
Com reacção ksantoproteinovaya é determinado aminoácido triptofano heterocíclico, indol possuindo um núcleo aromático. A presença dos compostos acima na proteína dá a mudança de cor característica do ambiente de teste.
Que reagentes uso
Para a realização da reacção ksantoproteinovaya precisa para preparar uma solução a 1% de proteína de ovo, ou de origem vegetal.
Normalmente usado ovo, o qual é dividido por uma separação adicional da proteína da gema. Para uma solução de 1% de proteína foi diluído em uma quantidade dez vezes maior de água purificada. Após a dissolução do líquido proteína resultante deve ser filtrada através de várias camadas de pano de queijo. Esta solução deve ser armazenado em local fresco.
É possível efectuar a reacção com uma proteína vegetal. Para preparar a solução é utilizada farinha de trigo numa quantidade de 0,04 kg. 0,16 l de água purificada. Os ingredientes foram misturados num balão que está ligado durante 24 horas num local fresco a uma temperatura de cerca de + 1 ° C. No final do dia, a solução foi agitada, seguido por filtração do mesmo primeiro com lã de algodão e, em seguida, – um filtro de papel dobrado. O líquido resultante foi mantida em um lugar fresco. Esta solução está presente principalmente na fracção de albumina.
Para levar a cabo a reacção ksantoproteinovaya como o principal reagente utilizado ácido nítrico concentrado. Outros reagentes é uma solução de hidróxido de sódio a 10% ou de amoníaco, a solução de gelatina e f enol não concentrado.
A metodologia do
Em um tubo limpo é feita 1% de solução de proteína de ovos -TH ou farinha numa quantidade de 2 ml. Para isto é adicionado cerca de 9 gotas de ácido nítrico concentrado a floculação parado. A mistura resultante foi aquecida, resultando precipitado amarelo desaparece gradualmente e a sua cor entra em solução. 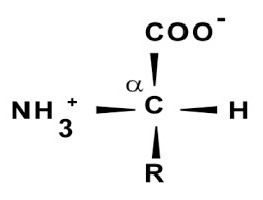
Quando o líquido arrefece no tubo ao longo da parede adicionado cerca de 9 gotas de hidróxido de sódio, concentrada, que é o excesso para o processo. O meio reaccional torna-se alcalina. Conteúdo torna-se cor de laranja no tubo de ensaio.
características do
Desde ksantoproteinovaya chamada reacção qualitativa de ácido nítrico pela acção das proteínas, a amostra é realizada sob incluídos hotte. Observe todas as precauções de segurança quando se trabalha com substâncias cáusticas concentradas.
A libertação dos conteúdos do tubo pode ocorrer durante o processo de aquecimento que tem de ser considerado quando se fixa-lo num suporte e seleccionando a inclinação.
De discagem de ácido nítrico concentrado e soda cáustica só deve utilizando uma pipeta de vidro e peras borracha pipeta proibido pela boca.
Relativa reacção com fenol
Para maior clareza, o processo e confirmação da presença dos grupos fenilo é realizada com uma amostra semelhante hidroxibenzeno.
O tubo de tomada de 2 ml de fenol diluído, depois, gradualmente, ao longo da parede, foi adicionado 2 ml de ácido nítrico concentrado. A solução foi submetida a aquecimento, pelo que se torna amarelo. Esta reacção é a qualidade da presença do anel de benzeno. 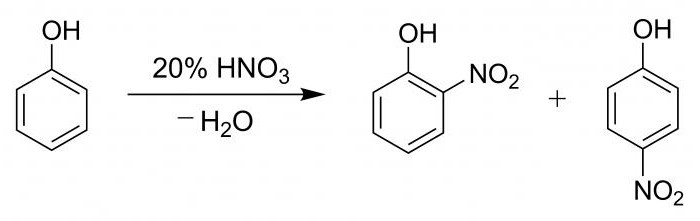
Processo hidroxibenzeno nitrado com ácido nítrico, seguida pela formação de uma mistura de p-nitrofenol e o-nitrofenol em uma percentagem de 15 a 35.
teste de comparação com a gelatina
Para provar que a reacção ksantoproteinovaya à proteína revela um aminoácido com estrutura aromática, utilizar as proteínas que não têm um grupo fenólico.
Em um tubo limpo é feita a solução de gelatina a 1% numa quantidade de 2 ml. Para isto é adicionado cerca de 9 gotas de ácido nítrico concentrado. A mistura resultante é aquecida. A solução não foi colorido de amarelo, o que prova a ausência de aminoácidos com uma estrutura aromática. Algumas vezes há um ligeiro amarelecimento do meio ambiente, devido à presença de impurezas de proteínas.
equações químicas
Na reacção de dois passos é executado ksantoproteinovaya proteínas. Fórmula primeiro processo de nitração fase descreve moléculas de aminoácidos, utilizando ácido nítrico concentrado.
Um exemplo disso é a ligação do grupo nitro para a tirosina para formar nitrotirosina e dinitrotirozina. No primeiro caso, para o anel de benzeno está ligado um -radical NO 2, e o segundo composto tem dois átomos de hidrogénio são substituídos por NO 2. Reacção química tirosina fórmula ksantoproteinovaya representado por reacção com ácido nítrico para formar molécula nitrotirosina.
processo de nitração é acompanhada pela transição de coloração, incolor, com tom amarelo. Na realização desta reacção com as proteínas que contêm os resíduos de aminoácido fenilalanina ou triptofano, e a cor da solução muda.
O segundo passo é o produto da reacção de nitração de moléculas de tirosina, especialmente nitrotirosina, com amónio ou hidróxido de sódio. O resultado é um sal de sódio ou de amónio, em que a cor amarelo-alaranjado. Este tipo de reacção está relacionada com a possibilidade de moléculas nitrotirosina mover sob a forma quinóide. Subsequentemente sal assim formado ácido Nitronic, que tem um sistema quinona de ligações duplas conjugadas. 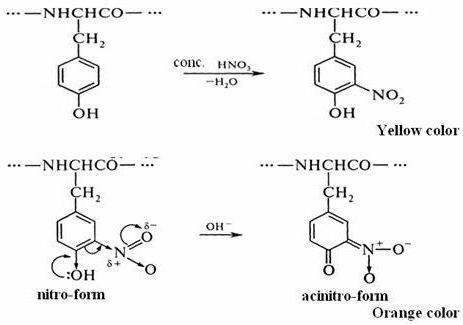
Assim termina reacção ksantoproteinovaya para proteínas. A equação acima apresentada segundo passo.
resultados
Durante a análise de fluidos contidos em três tubos, a solução de referência é diluída com fenol. As substâncias com um anel de benzeno dar reacção qualitativa com ácido nítrico. Como resultado, ele muda de cor da solução.
Como é sabido, a gelatina constitui uma forma de hidrolisado de colagénio. A proteína não contém a estrutura aromática dos aminoácidos. Nenhuma mudança em cor do meio de reacção com um ácido.
No terceiro tubo de ensaio, há uma reacção positiva para proteínas ksantoproteinovaya. Conclusão pode ser desenhada como se segue: todas as proteínas com estrutura aromática, quer se trate de um grupo fenilo ou um anel de indole, tendo em conta a mudança de cor da solução. Isto é devido à formação de compostos nitro com uma cor amarela.
Efectuar uma reacção de cor revela a presença de várias estruturas químicas em aminoácidos e proteínas. EXEMPLO gelatina mostra que a sua composição inclui ácido aminocarboxílico não possuindo um grupo fenilo ou uma estrutura cíclica.
Com ksantoproteinovaya reacção pode ser explicado pelo amarelecimento da pele, quando aplicado a ele um forte ácido nítrico. A mesma cor vai se tornar o leite espumoso durante sua análise semelhante.
Na prática laboratório clínico esta amostra de cor não é utilizado para a detecção de proteínas na urina. Isto é devido a cor amarela da própria urina.
Ksantoproteinovaya reacção tornou-se cada vez mais usado para a quantificação de ácidos aminados, tais como o triptofano e tirosina, como parte de várias proteínas.