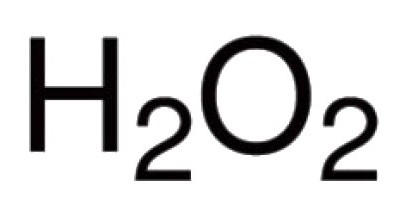Qual é a valência de oxigênio em compostos?
De modo a determinar o possível oxigénio valores de valência deve examinar a situação do elemento na tabela periódica, as principais características da estrutura dos seus átomos. Essa abordagem é útil no estudo da questão do que a valência de oxigênio no típico eo que não é típico para ele. Os compostos mais comuns apresentam a valência normal – II. Este recurso permite que você defina o número de ligações de outro átomo nas fórmulas binários acabados envolvendo oxigênio.
Qual é a valência de oxigênio no?
Na fase inicial de acumulação do conhecimento das propriedades e estrutura de substâncias químicos pensou que a valência – a capacidade de se ligar a um determinado número de átomos de uma molécula da substância. Muitos cientistas após a descoberta do elemento têm tentado entender o que a valência de oxigênio no. Resposta foi obtida por meio de experiências: oxigénio atribui átomo de hidrogénio dois monovalente numa reacção química, significa divalente. Representações de ligação química variada com a acumulação de conhecimento sobre a estrutura de substâncias. Na sua teoria da valência de H. Lewis e W. Kossel revelar a natureza da interacção química com a estrutura ponto de vista electrónico. Os investigadores explicam a capacidade do átomo para formar um certo número de conexões esforçando-se para o estado de energia mais estável. No caso de conseguir o menor de partícula da substância se torna mais estável. Na teoria e estruturas de Lewis muita atenção dada ao papel dos elétrons externos que participam na criação de uma ligação química.
Propriedades de colocação de oxigênio na tabela periódica
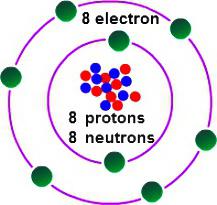
A fim de determinar aqueles que têm a valência de oxigênio, é preciso considerar algumas características de sua estrutura eletrônica. grupo de cabeça de oxigênio 16 da tabela periódica. O nome comum dos membros da família – "Calcogênios" de classificação ultrapassada a que pertencem grupo VI (A). Na tabela periódica de oxigénio se encontra numa célula sob №8. O núcleo contém na sua composição 8 e o mesmo número de partículas elementares neutras positivos. No espaço de um átomo, existem dois níveis de energia que ocorrem quando electrões 8, 6 dos quais – a externa.

O que existe relação entre a composição do átomo e a valência?
No último nível do átomo de oxigênio contém dois elétrons desemparelhados. O elemento de flúor é menor do que o valor de electronegatividade (capacidade para atrair electrões de ligação dupla). Na formação dos compostos com outros elementos de oxigénio atrai surgido na molécula uma densidade de electrões total (excepto electrões de flúor). Atingindo um estado de equilíbrio da casca exterior, possivelmente, com a adição de duas cargas negativas. Isto significa que é necessário oxigénio 2 electrões. Possíveis seguintes opções: aceitar um electrão (valência II), afastando-se os outros átomo de 2 electrões (valência II), não aceitar electrões de outros átomos (0) de valência. comportamento típico de oxigénio caracteriza o segundo caso. Desta forma, você pode usar para descobrir o que a valência de oxigênio no mais típico em seus compostos comuns. Estes incluem a maioria dos óxidos de metais e não-metais.
Como é que uma valência em compostos?
O oxigênio é capaz de interagir diretamente com muitos dos elementos químicos. Conhecido seus compostos com praticamente todos os representantes da tabela periódica (excepto para a gases inertes árgon, hélio, néon). A reacção com halogéneos e metais nobres, oxigénio não pode engatar directamente, mas óxidos Au 2 O 3, F 2 O, Cl 2 O 7 e existem outros (indirectamente obtido). Para os compostos binários na formação de oxigénio que faz parte, caracterizado por uma ligação covalente e polaridade. Valência em tais moléculas depende do número de quaisquer pares de electrões, que são atraídos para o núcleo de átomos diferentes. Na grande maioria dos compostos dos átomos de oxigénio estão envolvidos na criação de duas ligações covalentes. Por exemplo, nos óxidos de CO 2, P 2 O 5, SO 2, SO 3, K 2 O, B 2 O 3, Mo 2 O 5, e de outras moléculas. As exposições hidrónio catião H 3 O + oxigénio atípicas para ele valência III. A presença de peroxo -OO- causada natureza invulgar de peróxido de hidrogénio H 2 O 2. Este composto exibe uma característica de oxigénio que valência II.
Como determinar a valência dos elementos?
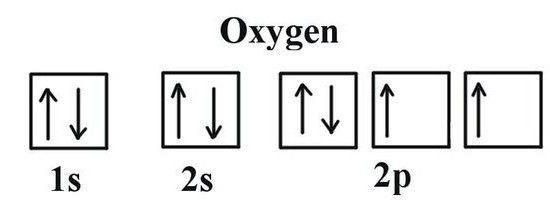
O conceito de oxigénio valência dá possibilidades estrutura de Lewis – símbolo químico elemento em torno do qual os electrões pontos marcam a camada exterior. Eles tomam parte na criação de moléculas que fazem parte dos pares de elétrons compartilhados. Fórmula Lewis demonstra valência de oxigénio correspondente para o número de seus electrões desemparelhados (2). O mesmo resultado foi obtido usando estruturas electrónicas de imagens. As duas células do nível de oxigénio externo electrões desemparelhados localizados (indicadas pelas setas na fórmula). Para obter informações sobre o que a valência do oxigénio em, permitindo que a fórmula final para o valor de um composto binário de átomos vizinhos. Para fazer isso, realizar cálculos simples. É primeiro multiplicado pelo número de átomos de O para a taxa normal para a valência de oxigénio. O valor resultante é dividido pelo índice, tal como especificado na fórmula, com o símbolo químico perto de um outro elemento, em combinação com oxigénio. Com um método simples que calcular o carbono e fósforo na valência seus óxidos.
- Multiplicar o índice no canto inferior direito do dióxido de sinal O em típico elemento de valência 2 CO 2 • 2 = 4. O número resultante para dividir índice especificado para o carbono: 4/1 = 4. O dióxido de carbono CO2 é no seu mais elevado estado de valência IV .
- Índice de canto inferior direito do símbolo química de oxigénio em óxido de fósforo P 2 O 5 multiplicam o átomo de valência O típico 5 • 2 = 10. Este número dividir pela referida fmula no índice no canto inferior direito dos átomos de fósforo: 10/2 = 5. O óxido de fósforo ele está no seu ápice V. valência